Фракционированная перегонка
Фракционированная перегонка, или дистилляция. Издавна известно, что температура кипения жидкости под постоянным давлением является одной из физических постоянных, характеризующих данное химическое соединение, температура же кипения растворов жидкости в жидкости находится в зависимости от относительного состава смеси или растворов. Теория фракционированной перегонки в настоящее время представляется в следующем виде (ср. перегонка, XXXI, 483).
1) Две несмешивающиеся жидкости, например керосин и вода, хлороформ и вода и т. п. Еще Реньо показал, что в случае, если мы имеем несмешивающиеся жидкости, образующие два слоя, и будем их нагревать, то каждая из них образует столько пара, сколько образовалось бы, если бы другой не было, и, таким образом, общее давление в пространстве, занятом парами, равно сумме обоих парциальных давлений. Нужно только, чтобы обе жидкости от времени до времени находились на поверхности, что достигается встряхиванием или перемешиванием жидкостей. Две таких жидкости вместе будут кипеть ниже, чем каждая в отдельности, так как сумма парциальных давлений пара обоих жидкостей достигает атмосферного давления при более низкой температуре, чем какая-либо из жидкостей. Перегонка начнется при температуре, при которой сумма парциальных давлений паров будет равна атмосферному давлению. Например, при 90,23° упругость паров воды равна 530,1 мм., а для хлоробензола — 210 мм, общая же упругость — 740,2 мм; опыт же показывает, что при давлении 740 мм смесь перегоняется при температуре от 90,25° до 90,35° до тех пор, пока в перегонном аппарате находятся обе жидкости. Когда же хлоробензол будет отогнан, температура быстро поднимается до 100°. Равным образом, если на бромоформ, кипящий при 151°, налить тонкий слой воды, то кипение начинается при 93°, ибо уже при этой температуре сумма давлений паров воды и бромоформа равна атмосферному давлению. Бензойно-кислый этил кипит при 213°, упругость пара его при 100° = 16 мм ртутного столба, и этого достаточно, чтобы смесь бензойного этила и воды кипела почти на целый градус ниже 100°. Точка кипения остается неизменной, пока имеется достаточное количество обоих жидкостей. Состав дистиллята двух не смешивающихся жидкостей остается неизменным до тех пор, пока не отгонится вполне та или другая жидкость: количество каждой жидкости, находящееся в парах, пропорционально упругости этой жидкости и не зависит от относительных количеств жидкостей, находящихся в реторте, из которых перегоняют жидкости. Если (М1, М2, Р1, Р2) обозначают молекулярные веса и давления пара жидкостей А и В, то отношение между количествами А и В, перешедшими в дистиллят равно М1Р1:М2Р2.
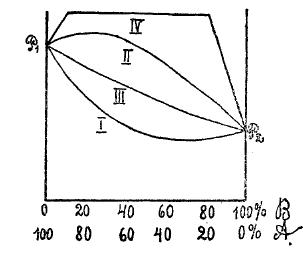
В общем случае, когда одна жидкость (например, А) более летуча, чем другая (например, В), т. е. Р1 больше, чем Р2, молекулярный же вес M1 много меньше, чем М2, то ясно, что отношение M1 P1:М2Р2 не может быть очень большим, и менее летучая жидкость В может отгоняться в значительном количестве. На этом основана перегонка с помощью водяного пара, где относительно большая летучесть воды уравновешивается относительно высоким молекулярным весом другого тела; например, в случае нитробензола и воды отношение между перегоняющимися количествами бензола и воды = 1:5. Вообще, когда тело обладает упругостью пара только 10 мм при 100°, то для отгонки его может быть применена перегонка с водяным паром. В том случае, если две жидкости смешиваются между собой до известной степени, например, эфир и вода, то получаются два раствора: 1) водный раствор эфира и 2) эфирный раствор воды. Упругость пара, равно как и относительные количества составных частей паров, выделяющихся из обоих насыщенных растворов, как показал Д. П. Коновалов, одинаковы. В этом случае, упругость пара раствора сперва растет, достигает максимума и остается постоянной, когда имеем одновременно два слоя насыщенных растворов, а затем постепенно уменьшается (см. кривая IV на рис.).
2) Наиболее сложные отношения наблюдаются над упругостью пара двух совершенно смешивающихся жидкостей. Если мы к жидкости А прибавим небольшое количество жидкости В, то произойдет с одной стороны, уменьшение упругости пара жидкости А, с другой стороны — увеличение общей упругости пара раствора, ибо растворенная жидкость В, в свою очередь испаряется, и парциальное давление ее пара тем больше, чем менее коэффициент растворимости ее паров в жидкости А. Смотря по тому, какое действие преобладает, упругость пара раствора будет больше или меньше упругости пара жидкости А.
То же самое произойдет, если мы к жидкости В прибавим небольшое количество жидкости А, и упругость пара происшедшего при этом раствора будет выше или ниже упругости пара жидкости В; при этом могут быть различаемы три типические случая:
I. Пар жидкости А легко растворяется в жидкости В и обратно (В в А и А в В). При небольшой примеси В к А упругость пара раствора понижается. Если мы будем прибавлять к жидкости А последовательно увеличивающиеся количества В то упругость пара раствора будет постепенно уменьшаться, достигнет минимума и затем, постепенно возвышаясь, при очень большом избытке В, приблизится к упругости пара В, Р2.
На рис. кривая I изображает изменение упругости пара раствора А—Р1 и В—Р2.
Такой вид представляют кривые упругости пара водных растворов муравьиной кислоты. Кривая (при 100°) вогнута и почти на всем своем протяжении опускается ниже обоих крайних пунктов; она имеет ясно выраженный минимум, который соответствует приблизительно 30% содержания воды; при других температурах она имеет подобный же вид.
II. Пар А растворим незначительно в В, и обратно — пар В мало растворим в А. Поэтому при прибавлении небольшого количества А к В, и обратно — В к А упругость пара раствора будет повышаться. При последовательном прибавлении к А упругость пара раствора растет, затем достигает максимума, от которого, понижаясь, приближается к упругости пара В,—Р2. Кривая II представляет упругость пара подобных растворов. Кривая упругости пара водных растворов пропилового спирта совершенно сходна с кривой II. Упругость пара раствора больше упругости пара его компонентов. Кривая достигает максимума при 25% спирта.
III. Пар одной жидкости легко растворим в другой, пар же второй в первом растворим трудно. При небольшом прибавлении В к А упругость пара происшедшего раствора меньше, при небольшом прибавлении А к В, напротив, больше упругости пара чистого растворителя.
Если упругость пара А (Р1) больше упругости пара В (Р2), то, при последовательном прибавлении В к А, упругость пара без ясно выраженного максимума и минимума переходит от Р1 к Р2 (кривая III). К подобному роду кривой подходит кривая упругости пара водных растворов метилового спирта.
На основании кривых упругости пара растворов можно видеть, что растворы будут вести себя при перегонке следующим образом:
А. Растворы, кривая упругости пара которых не имеет ни максимума, ни минимума. Состав жидкости будет постоянно изменяться, температура повышаться, и состав остающегося раствора все больше и больше будет приближаться к составу выше кипящей жидкости. Конечный результат повторной перегонки — полное разделение жидкостей. Это случай, наиболее часто встречающийся в лабораторной и заводской практике.
В. Растворы, кривая упругости пара которых имеет максимум, т. е. температура кипения раствора на всем протяжении кривой ниже средней температуры кипения составных частей, точка же кипения раствора, соответствующего максимуму, лежит ниже температуры кипения наиболее летучей жидкости. При перегонке подобного раствора произвольного состава температура возвышается, и в перегонном сосуде остается жидкость все более и более удаленная по своему составу от раствора, в дистиллят же переходит часть, приближающаяся к раствору, соответствующему максимуму. Если подвергать первые порции дистиллята повторной перегонке, то можно получать, в конце концов, раствор с наибольшей упругостью пара. Этот раствор при дальнейшей перегонке не будет разлагаться.
При повторных перегонках остатка получается, наконец, одна из жидкостей в чистом виде, а именно та, которая находится вместе с первоначально взятым раствором по одну сторону от максимума. К этой группе относятся водные растворы пропилового спирта и масляной кислоты. Для пропилового спирта раствор его (77% спирта и 28% воды) представляет нераздельно кипящую смесь. При перегонке раствора масляной кислоты, содержащего около 17 частей кислоты и 100 воды, кипение начинается при 99°,8; первый дистиллят содержит около 20 частей кислоты, следующая порция (температура кипения 99°,9) содержит около 14 частей, наконец, температура поднимается до 100°, и дистиллят состоит почти из чистой воды. Таким образом, масляная кислота, кипящая при 163°, перегналась в первых порциях перегонки, оставив в остатке воду. При повторной перегонке первых порций дистиллята возможно выделить нераздельно кипящий при 90°,5 раствор 23 частей кислоты в 100 частях воды.
При перегонке же раствора, содержащего около 40% кислоты, температура кипения (в начале 99°,6) постепенно поднялась и, наконец, достигла 163°. Остаток в колбе состоял из чистой масляной кислоты. Из первых порций дистиллята был и здесь выфракционирован тот же нераздельно кипящий раствор, что и в предыдущем случае.
С. Растворы, для которых кривая упругости пара имеет минимум (т. е. раствор, соответствующий минимуму, кипит выше наименее летучей из жидкостей). Дистиллят, удаляясь от минимума, будет приближаться по составу, к одной из жидкостей, остаток все более и более будет приближаться к составу раствора с наименьшей упругостью пара. Этот раствор дальнейшей перегонкой разлагаться не будет.
Таким образом, продуктом повторной перегонки будет нераздельно кипящий раствор и чистая жидкость, лежащая вместе с первоначально взятой смесью по одну сторону от минимума.
Ив. Каблуков.
| Номер тома | 44 |
| Номер (-а) страницы | 427 |
