Химия. Химия биологическая
XI. Химия биологическая, или биохимия, или физиологическая химия является наукой о химии жизненных процессов, изучает химическую статику и динамику животных и растительных организмов. Она связана с химией и сама является химической наукой, ибо пользуется химическими и физико-химическими методами исследования, изучает химические и физико-химические процессы, происходящие в теле животных и растений. С другой стороны, химия биологическая тесно связана с физиологией (как общей, так и частной), ибо она изучает только те процессы, которые совершаются в живой природе, только те химические вещества, которые входят в состав клеток тела животных и растений.
Биологическая и физиологическая химия — два почти равнозначащих названия; несколько более широким является название — биохимия, ибо оно охватывает все вообще химические вопросы биологии; круг задач физиологической химии обычно ограничивается изучением химической и физико-химической статики и динамики животного организма, ибо химические процессы, происходящие в растениях, равно как и химическая статика растительных клеток, составляют обычно предмет физиологии растений и описываются в руководствах по физиологии растений в соответствующих их главах, например дыхание растений, питание растений и т. п.
Химия физиологическая обычно затрагивает химию растений постольку, поскольку это необходимо для понимания того, что происходит в теле животных и человека.
Химия биологическая прежде всего изучает химические элементы, принимающие участие в образовании того материала, из которого построены живые существа - животные и растения. В ее задачи входит проследить все превращения, в которых участвуют эти элементы, когда они из мертвой природы поступают в живую, в ней становятся материалом для построения частей тела животных и растений и когда они, наконец, снова возвращаются в мертвую природу. Говоря другими словами, одной из задач химии биологической является изучение круговорота химических элементов в природе, раскрывающее нам картину химических взаимоотношений между животными и растениями, между живой и мертвой природой. Все химические элементы, служащие материалом для построения живых организмов, поступают в них из мертвой природы; в живых организмах эти элементы идут на образование более или менее сложных химических соединений. Эти соединения подвергаются различным превращениям в клетках растений и животных; в конце концов, они разлагаются, и входивший в их состав химический элемент снова возвращается в мертвую природу. Таков круговорот всех элементов, входящих в состав растений и животных; таков, например, круговорот азота, углерода, серы и т. д. О круговороте азота см. ассимиляция азота. Что касается углерода, то он поступает в растения в виде углекислого газа (СО2), который растения забирают из воздуха. В растениях из этого углерода строятся разнообразные органические соединения, которые из растений поступают в тело травоядных животных, а из него в тело плотоядных. Органические углеродистые соединения в теле животных окисляются и, в конце концов, входивший в их состав углерод снова поступает в воздух в виде СО2.
Следующая задача химии биологической заключается в изучении химического состава живых организмов. Это изучение химической статики живых существ является основной предпосылкой для изучения их химической динамики, т. е. для изучения химических и физико-химических процессов, совершающихся в теле животных и растений с теми веществами, из которых были построены отдельные его клетки, или которые поступили из него в виде пищи. Поэтому в первый период развития биохимии главное внимание и было обращено на изучение состава отдельных частей тела животных и растений. Это изучение не закончено и теперь, ибо органические вещества, из которых построены живые клетки, являются очень сложными веществами, а изучение их может считаться законченным только тогда, когда будет выяснен в деталях не только их состав, но и структура, и когда данные о структуре будут проверены путем их синтеза.
Из главных групп органических веществ, входящих в состав строительного материала клеток нашего тела, равно как клеток тела животных и растений, лучше изучены жиры, ибо мы знаем состав и структуру нейтральных жиров и можем их синтезировать. Но уже структура близких к жирам веществ-фосфатидов (например, лецитины, см.) и стеринов (например, холестерин, см.) в деталях еще не выяснена и является сейчас предметом интенсивного изучения. Так же обстоит дело с углеводами и белками. Относительно структуры полисахаридов — крахмала, гликогена, клетчатки — известно, что их молекулы построены из нескольких молекул моносахаридов - гексоз, именно из молекул глюкозы (С6Н12О6).
До недавнего времени думали, что молекулы глюкозы соединены между собой в молекуле крахмала так же, как и в молекуле ди- и трисахаридов, т. е. что молекула крахмала построена в виде цепи из остатков глюкозы. Исходя из представлений о такой структуре крахмала, нельзя было объяснить ряда его свойств и понять механизм его превращений (расщепление). И вот теперь, благодаря новейшим исследованиям Karrer, Pringsheim, Irvine и др., мы знаем, что структура полисахаридов иная. Они построены из нескольких кольцевых комплексов, соединенных между собой вторичными связями. Такими кольцевыми комплексами в молекуле крахмала являются диамилозы и триамилозы. Диамилоза построена из остатков двух молекул глюкозы, которые, соединяясь между собой, потеряли две молекулы воды (а не одну, как это бывает при образовании из двух молекул глюкозы мальтозы). Образование диамилозы, поэтому, изображается так:
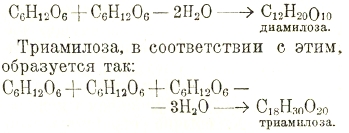
Pringsheim считает, что одна составная часть крахмала — амилопектин построен из нескольких соединенных между собой молекул (кольцевых) триамилозы, а другая составная часть — амилоза построена из частиц диамилозы.
Вот какова структура диамилозы и триамилозы и вот как они, по мнению Pringsheim’а, соединяются между собой в молекуле крахмала:

Соединение триаиилозы и диамилозы в молекуле крахмала.
Аналогичную структуру имеют и гликоген и клетчатка. Исследования над структурой крахмала показали, что молекулярный вес его вовсе не так велик, как думали раньше, и выяснили нам далее механизм образования мальтозы при гидролизе крахмала, показав, что образование мальтозы при расщеплении крахмала происходит путем синтеза из остатков глюкозы, освобождающихся при разрыве диамилозного кольца.
Аналогичную судьбу испытали и наши представления о структуре белков. После исследований Э. Фишера, выяснивших структуру полипептидов и показавших, что полипептиды находятся всегда среди продуктов постепенного гидролиза белков (среди пептонов), считали, что белки построены по типу полипептидов, т. е. что молекула белков имеет вид цепи из остатков аминокислот, соединенных между собой так, как они соединены в молекуле полипептидов. Однако, вскоре оказалось, что, допуская такую структуру белков, мы не можем объяснить ряда их свойств. И вот новейшие исследования над структурой белков, например исследования Abderhalden, Troensegaard, Bergmann, Karrer, Herzog, Brigl, — все говорят за то, что в молекуле белков должны быть соединения кольцевой структуры (или пиперазиновые кольца, или оксипирроловые, или окзазолиновые и т. д.) и что, может быть, молекула белка построена аналогично молекулам полисахаридов и состоит из нескольких связанных между собой кольцевых соединений. Эти исследования чрезвычайно интересны и не только с точки зрения изучения химической статики, но и потому, что дадут нам возможность понять некоторые пока еще темные стороны белкового обмена.
Вообще знание химического состава и структуры веществ, из которых построены разные части тела растений и животных, необходимо для изучения их обмена. Физиологическая химия ставит себе задачей изучение во всех деталях превращений веществ в животном организме; мы должны знать, что делается, например, с каким либо веществом, поступающим в наше тело в составе пищи, от момента его поступления в ротовую полость до момента выделения конечных продуктов его обмена.
Углеводы, жиры и белки в органах пищеварения подвергаются гидролитическому расщеплению, вызываемому соответствующими ферментами-гидролазами, содержащимися в пищеварительных соках — слюне, желудочном соке, панкреатическом и кишечном соке (см. пищеварение). В результате гидролиза все эти вещества распадаются на структурные элементы их молекул, которые и всасываются. Таким образом, благодаря пищеварению пищевые вещества, с одной стороны, превращаются в растворимые в воде вещества, которые могут всосаться, а с другой стороны — теряют свой специфичный состав и структуру, превращаясь во вполне индифферентные вещества.
За последние годы достигнуты очень большие успехи в деле выяснения дальнейшей судьбы всосавшихся продуктов, выяснения тех химических превращений, которым эти вещества подвергаются в клетках тела животных. В результате всасывания углеводов, по ту сторону органов пищеварения, в кровеносной системе, оказывается глюкоза; она частью подвергается немедленному потреблению в клетках тела, частью отлагается про запас в печени и мышцах в виде гликогена с тем, чтобы он впоследствии превратился в глюкозу и был использован животным организмом. Углеводы являются источником мышечной силы, и главным местом, где тратятся углеводы, где они (глюкоза) подвергаются дальнейшим превращениям, являются мышцы. Распад глюкозы в мышечных клетках проходит всегда через ряд определенных промежуточных этапов, причем исследования последних лет (Neuberg и др.) показали, что превращения углеводов происходят одинаково и в мышечных клетках высших животных и при спиртовом брожении, вызываемом дрожжевыми клетками, т. е. одноклеточными организмами. И там, и здесь процесс начинается с образования соединения глюкозы с фосфорной кислотой (гексозофосфорная кислота, лактацидоген Эмбдена), которое затем распадается на фосфорную кислоту и глюкозу; и там и здесь эта глюкоза, распадаясь и окисляясь, превращается шаг за шагом в одни и те же промежуточные продукты; и только в самом конце пути расходятся. Уксусный альдегид, образующийся в качестве промежуточного продукта в обоих случаях, при спиртовом брожении восстанавливается в этиловый спирт, а при обмене глюкозы в мышечной ткани окисляется в уксусную кислоту и далее в СО2 и Н2О. Весь ход обмена глюкозы можно представить следующей схемой:
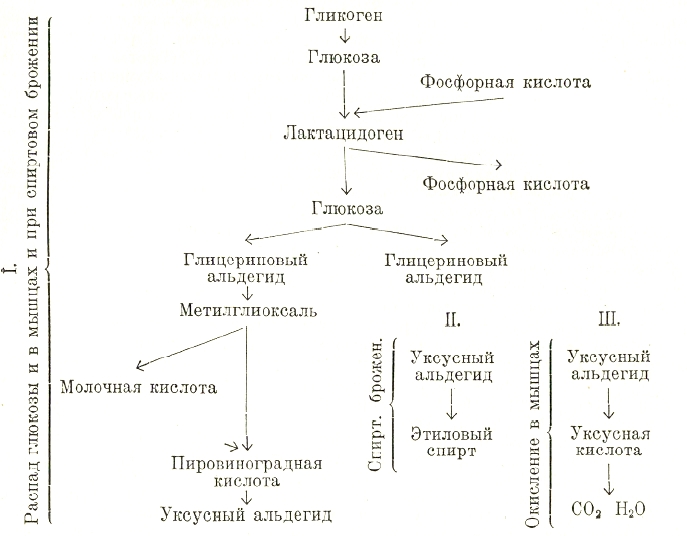
Все эти превращения углеводов осуществляются при участии ряда ферментов, среди которых одно из главных мест выпадает на долю оксидоредуказ. Все ферменты углеводного обмена, кроме ферментов гидролизирующих полисахариды и дисахариды, Орреnheimer и Neuberg относят к группе десмолаз. Из отдельных ферментов, катализирующих ту или иную стадию углеводного обмена, можно указать кетональдегидмутазу (Neuberg), превращающую метилглиоксаль в молочную кислоту:
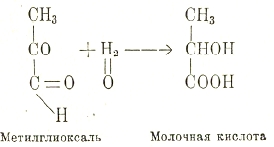
далее, карбоксиллазу, под влиянием которой от пировиноградной кислоты отщепляется СО2 и образуется уксусный альдегид:
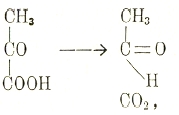
оксидоредуказу, восстанавливающую метилглиоксаль в пировиноградную кислоту и т. д.
Выяснение всех промежуточных этапов, через которые проходит обмен углеводов, дало возможность понять механизм превращения одних веществ в другие, например углеводов в жиры, белков в углеводы. Оказалось, что и при обмене жиров и при обмене белков могут образоваться в качестве промежуточных продуктов такие же вещества (или очень близкие к ним), какие образуются при обмене углеводов. Ясно теперь, что, например, распад углеводов может дойти до какого-либо продукта, который может образоваться и при распаде жиров, а с этого момента процесс может повернуть в сторону образования составных частей молекулы жиров (глицерина и жирных кислот) и даже самих жиров.
Процессы внутриклеточного обмена нейтральных жиров или, лучше сказать, глицерина и жирных кислот (ибо первым этапом превращения жиров является их распад на глицерин и жирные кислоты) изучены в настоящее время довольно хорошо. Глицерин при внутриклеточном обмене может дать такие же промежуточные продукты, в которые превращается глицериновый альдегид, образующийся при распаде глюкозы. Механизм внутриклеточного (интермедиарного) обмена жирных кислот изучил, главным образом, Knoop, который установил, что превращение жирных кислот идет путем р-окисления, т. е. путем β-окисления углеродного радикала, находящегося в β-положении по отношению к карбоксилу, и отщепления при этом двух углеродных радикалов (карбоксила и соседнего е ним α-радикала) в виде уксусной кислоты. Благодаря этому жирная кислота укорачивается на два углеродных радикала; образовавшаяся кислота с укороченной углеродной цепью в свою очередь подвергается β-окислению и снова укорачивается на два углеродных радикала и т. д. В конце концов из жирных кислот с четным числом углеродных атомов в частице образуется масляная кислота, которая, подвергаясь β-окислению, расщепляется на две молекулы уксусной кислоты. Превращение этой последней, проходя через образование ряда промежуточных продуктов, заканчивается в конце концов так, что входящий в ее состав водород окисляется до воды, а углерод — до СО2.
Таким образом, превращение жирных кислот в животном организме проходит такие фазы: .
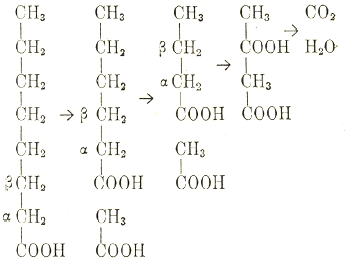
Механизм β-окисления таков, что насыщенная жирная кислота сперва превращается в ненасыщенную, затем в оксикислоту, далее в кетонокислоту, которая и распадается, присоединяя, воду, на уксусную кислоту и жирную кислоту, имеющую углеродную цепь более короткую, чем имела исходная кислота; словом, β-окисление проходит через следующие этапы:
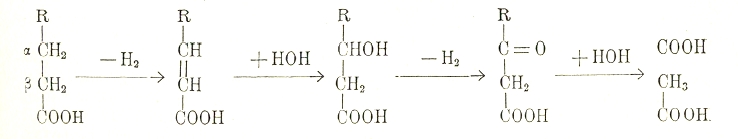
Из этого видно, что при промежуточном обмене жиров действительно образуются или такие продукты, какие образуются при обмене углеводов, или такие, какие легко могут образоваться из промежуточных продуктов углеводного обмена и обратно.
В результате переваривания белков пищи в органах пищеварения, в кровеносной системе (после всасывания), оказываются аминокислоты; они же образуются в каждой клетке тела при распаде белков. Аминокислоты занимают центральное место в белковом обмене, такое же как гексозы — в углеводном. Поэтому, желая изучить процессы внутриклеточного обмена белков, мы должны изучить обмен аминокислот. Появятся ли в какой-либо клетке тела аминокислоты в результате распада ее белков, или они поступят в нее из крови, попав в последнюю из кишечника, механизм превращения их будет одинаков.
Первым этапом обмена аминокислот является их дезаминирование, т. е. потеря аминогруппы, которая отщепляется в виде NH3 (аммиака). Это дезаминирование происходит окислительным путем. Knoop, принимая теорию окислений Wieland’а, считает, что первым этапом окислительного дезаминирования является отщепление Н2 и превращение аминокислоты в иминокислоту:
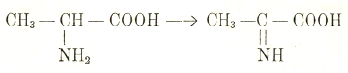
Иминокислота, присоединяя воду и теряя NH3, превращается в кетонокислоту:
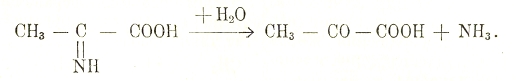
Механизм дальнейших превращений кетонокислот таков же, какой имеет место при процессах промежуточного обмена углевода, когда кетонокислота (пировиноградная) теряет под влиянием фермента карбоксилазы СО2 и превращается в альдегид. Альдегид, далее, окисляется в соответствующую кислоту, а она подвергается затем таким же превращениям, как это вообще свойственно жирным кислотам, т. е. окисляется по правилу Knoop’а.. Снова мы видим, что при процессах внутриклеточного обмена белковых веществ (аминокислот) образуются те же самые промежуточные продукты, что и при обмене углеводов и жиров (или близкие к ним).
Еще недавно господствовало мнение, что только растения могут синтезировать белковые вещества (т. е. сперва аминокислоты), используя для этой цели неорганические соединения азота; за животными же признавали способность образовывать белки только из органических соединений азота. Но уже несколько лет тому назад Knoop показал, что в теле животных может идти образование аминокислот из кетонокислот и аммиака. Эти данные были подтверждены Embden’oм в опытах с переживающей печенью; все же казалось, что этот синтез не может играть большой роли в животном организме. И вот теперь Knoop окончательно доказал, что процесс окислительного дезаминирования аминокислот, при котором они распадаются на кетонокислоты и аммиак, является обратимым процессом, подобно тому как обратимы процессы распада глюкозы и распада жирных кислот. Дезаминирование аминокислот является реакцией окисления; синтез аминокислот из аммиака и кетонокислот (аминирование кетонокислот) является реакцией восстановления. При этом синтезе, как и при дезаминировании, в качестве промежуточного этапа образуется, по мнению Knoop’а, иминокислота. Этот «восстановительный» синтез не может считаться редко встречающимся в животном организме, ибо Knoop показал, что он легко стимулируется теми факторами, которые в животном организме вообще стимулируют реакции восстановления. Из этих данных вытекает, что и в животном организме имеет место синтез аминокислот из неорганических соединений азота (аммиака). Таким образом, еще одно принципиальное отличие животного и растительного организма оказывается несуществующим.
Наряду с изучением химической динамики обмена веществ в животном организме химия биологическая имеет своей задачей изучение физико-химических условий жизни клеток и физико-химических процессов, в них развертывающихся при жизни. Мы знаем, что для нормальной работы органов необходимы определенные физико-химические условия, в смысле определенной реакции среды (определенной концентрации водородных ионов), определенного осмотического давления (изотония), наличия определенных ионов и в определенном друг к другу соотношении (изоиония), определенного состояния коллоидов и т. д. Самые незначительные изменения в физико-химическом «status quo» могут вызвать изменения в работе клеток и органов, в ходе того или иного химического или физико-химического процесса, изменив состояние коллоидов клеток, степень их дисперсности, изменив явления адсорбции и т. д. Небольшие изменения в реакции, в концентрации водородных ионов могут сильно повлиять на работу ферментов-катализаторов, участвующих в каждом химическом процессе, из которых слагается весь обмен веществ в животном организме.
Изучение ферментов (см.), их свойств, химической природы, механизма ферментативных процессов является следующей, одной из наиболее важных задач химия биологической. Относительно химической природы ферментов мы и сейчас почти ничего не знаем, хотя за последние годы, благодаря работам Баха, Euler’а, Willstätter'а, достигнуты большие успехи в деле очищения препаратов ферментов, в деле получения ферментов свободными от всяких примесей, что является неизбежной предпосылкой для выяснения химической природы ферментов. Эти исследования показали, во-первых, что ферменты, которые раньше считали, например, за белковые вещества, после очистки (хотя бы и не совсем полной) оказывались не содержащими азота, а во-вторых, что по мере очищения ферментов менялись их химические и физико-химические свойства; поэтому старые данные об оптимальной реакции для данного фермента, об его электрическом заряде, установленные для неочищенных ферментов, не будут иметь силы для чистых ферментов.
Много внимания и работы последнее время уделяется изучению окислительных ферментов в теле животных. В этой области из более новых работ и теорий основными нужно считать исследования и теории А. П. Баха, В. И. Палладина, О. Warburg’а, и Н. Wieland'а. Эти исследования все более и более приводят нас к убеждению, что оксидазам, т. е. ферментам, катализирующим окисление за счет свободного кислорода, не принадлежит главная роль в окислительных процессах; большая, даже главная часть этих последних происходит при участии оксидоредуказ, когда одновременно с процессами окисления происходят и процессы восстановления. Оксидоредуказы катализируют окисление кислородом воды, восстанавливая в то же время водородом воды другое вещество, которое служит, таким образом, водородным акцептором. Бах дал этим ферментам название пергидраз. Wieland считает, что в основе окисления всегда лежит отнятие водорода, который немедленно присоединяется к другому веществу и его восстанавливает. Wieland также признает участие воды в оксидоредукциях, но в отличие от Баха и В. Палладина считает, что вода сперва присоединяется к подлежащему окислению веществу, которое превращается в гидрат; затем уже оксидоредуказа, или дигидраза, как ее называет Wieland, отщепляет Н2 от гидрата, этим его окисляя, и присоединяет этот водород к другому веществу (или к другой частице того же вещества), восстанавливая его.
По Баху, оксидоредукция уксусного альдегида идет так:
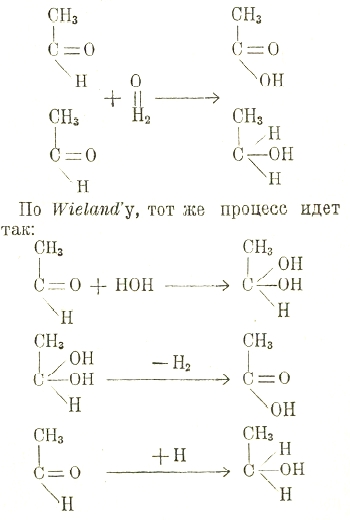
Процессы обмена веществ в теле животных регулируются, с одной стороны, гормонами — продуктами внутренней секреции эндокринных желез, а с другой стороны, витаминами — веществами, поступающими в тело животного с пищей (см. физиология питания).
Изучение химической природы гормонов и витаминов, их роли в организме и их влияния на процессы обмена веществ является опять-таки задачей химии биологической. Гормоны образуются в теле животного, витамины доставляются в него с пищей (главным образом растительной, ибо в растениях витамины образуются) и могут только при обильной доставке отлагаться в нем про запас. Изучение гормонов за последние годы быстрыми шагами идет вперед: недавно открыт инсулин, затем Callip выделил гормон околощитовидных желез, и теперь идет интенсивная работа над гормоном половых желез.
Витамины делят теперь (1927) на 5 групп: 1) антиксерофтальмические, или витамины А, 2) антиполиневритные, или витамины В, 3) антискорбутные, или С, 4) антирахитные, или витамины D, и 5) витамины размножения, или Е. Химическая природа витаминов нам пока неизвестна; только в отношении витамина D мы знаем, что это — вещество близкое к холестерину, ибо витамин D образуется из эргостерина при освещении его ультрафиолетовыми лучами (кварцевой лампой); близок к холестерину, по-видимому, и витамин А.
Далее химия биологическая ставит себе задачей изучение химической статики и динамики каждого отдельного органа тела животного, выяснение механизма его работы. Из этой области сейчас первоочередными являются исследования над биохимической динамикой мышц и над химической статикой и динамикой мозга. Благодаря работам Hill, Меуеrhoff, Embden химические процессы в мышцах при их покое и работе изучены настолько, что имеется возможность нарисовать довольно полную картину химизма мышечного сокращения.
Изучение биохимии головного мозга до недавнего времени шло исключительно по пути исследования химического состава всего мозга или отдельных больших его частей (серое и белое вещество). Теперь благодаря развитию микрометодики есть возможность изучать состав отдельных участков (центров) коры, и первые шаги в этом направлении показали, что в коре головного мозга наряду с топографией гистологической и функциональной имеется и топография химическая, т. е., что в составе отдельных центров коры имеются определенные различия. Далее, изучались изменения в составе мозга при тех или иных условиях и, наконец, стали появляться работы динамического характера, в которых изучалось, например, влияние разных факторов (голодания, раздражения, наркоза) на процессы протеолиза (распада белков) или во всем головном мозгу, или отдельно в сером и белом его веществе (Soula, А. Палладии). Развитие микрометодики дало возможность науке уточнить задачу и пойти по пути исследования динамики не всей коры, а отдельных ее центров; первые работы в этой области показали, что имеется определенная связь между работой зрительных центров коры и процессами протеолиза в них (Городисская). Эти данные являются первым экспериментальным доказательством наличия связи между функцией нервных центров коры и химическими процессами, протекающими в них. Все эти исследования кладут начало психохимии, науки, которая будет изучать химии психических процессов, и можно надеяться, что дальнейшая работа биохимиков в этом направлении и по этому пути приведет нас к выяснению механизма психической деятельности коры головного мозга.
Еще много и других задач стоит перед биохимией, например изучение химизма оплодотворения, выяснение того, как и какими веществами передаются наследственные признаки, работы по химии иммунитета и мн. др. Все это указывает, какое важное место занимает химия биологическая среди других наук; она является фундаментом медицинских наук и ряда наук биологических; она является базой и для общественных наук.
Литература: А. Палладин, «Учебник физиологической химии», 2 изд. 1927: Мейергоф, «Динамика жизненных явлений», 1926; «Успехи биологической химии», I—IV, 1924—26: Abderhalden, «Lehrbuch der physiologischen Chemie», 5 изд. 1924; Hammarsten, «Lehrbuch der physiolog. Chemie», 11 изд. 1926; Oppenheimer, «Handbuch der Biochemie d. Menschen und d. Tiere», 2 изд., тт. I—Х, 1924-27.
А. Палладин.
| Номер тома | 45 (часть 2) |
| Номер (-а) страницы | 368 |
