Малеиновая и фумаровая кислоты
Малеиновая и фумаровая (Ф) кислоты, НООС.СН = СН.СООН, две простейших непредельных двуосновных кислоты. Легко получаются из яблочной (оксиянтарной) кислоты отнятием воды: НООС.СН(ОН).СН2.СООН — Н2О = НООС.СН : СН.СООН. При медленном нагревании яблочной кислоты до 140°-150° образуется главным образом фумаровая кислота; при быстром — ангидрид малеиновой кислоты. Обе кислоты легко переходят друг в друга. Фумаровая кислота превращается в малеиновую под влиянием ультрафиолетовых лучей, а также при действии галоидных соединений фосфора. Обратно малеиновая кислота переходит в фумаровую при действии галоидов, особенно на солнечном свету, а также просто при продолжительном нагревании выше 140°. Обе кислоты при действии амальгамы натрия дают янтарную кислоту; присоединяя бромистый водород, переходят в монобром-янтарную кислоту, а при нагревании с водой — в яблочную кислоту. Естественно, что обеим кислотам, фумаровой и малеиновой, приписывают одно и то же строение. Между ними, однако, есть одно существенное различие. Тогда как малеиновая кислота, отщепляя воду, легко дает соответствующий ангидрид, фумаровая кислота не способна к образованию ангидрида. Различие это прекрасно объясняется со стереохимической точки зрения. Допускают, что карбоксилы, СООН, в малеиновой кислоте расположены по одну сторону плоскости, проходящей через углероды, соединенные двойной связью:
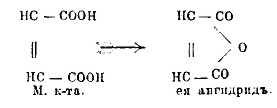
В фумаровой же кислоте группы СООН находятся по разные стороны той же плоскости:
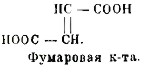
Фумаровая кислота.
Фумаровая кислота встречается во многих растениях (например, Fumaria officinalis); она трудно растворима в холодной воде; при 200° возгоняется, не плавясь. Малеиновая кислота в природе не встречается; легко растворима в холодной воде; плавится при 130°, а при 160° кипит, отщепляя воду с образованием малеинового ангидрида.
С. Наметкин.
| Номер тома | 28 |
| Номер (-а) страницы | 68 |
