Радиоактивность и радиоактивные вещества
Радиоактивность и радиоактивные вещества. В 1896 г., после открытия Х-лучей Рентгеном (см. рентгеновские лучи), Анри Беккерель (см.) поставил опыты для того, чтобы узнать, не испускают ли все фосфоресцирующие (см. ХХVІI, 535/37) вещества Х-лучей. Он нашел, что только фосфоресцирующие соединения урана, положенные на фотографическую пластинку, завернутую в черную бумагу, подобно Х-лучам, вызывали почернение пластинки. Впоследствии оказалось, что соли урана и без предварительного освещения, т. е. не в состоянии фосфоресценции, производят то же действие. После того как выяснилось, что соединения урана разряжают заряженный электроскоп, т. е. делают воздух проводником электричества, стало ясным, что уран и его соли испускают невидимые лучи, подобные рентгеновым лучам. М. Кюри (см.) продолжила исследования Беккереля и нашла, что из всех химических элементов, кроме урана, тем же свойством обладает только торий. Вместе с тем она показала, что эффект излучения в соединениях или смесях пропорционален количеству самого урана или тория, т. е. что свойство излучать невидимые лучи присуще атомам урана и тория. Это свойство она назвала радиоактивностью, а элементы, обладающие этим свойством, — радиоактивными (от radius — луч).
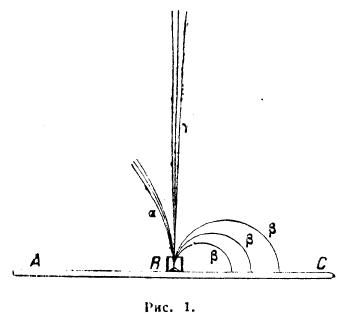
Рис. 1.
Дальнейшие опыты М. Кюри показали, что урановые руды в 4-10 раз радиоактивнее, чем можно было бы от них ожидать, судя по содержанию в них урана. В 1898 г. супруги П. и М. Кюри нашли, что отбросы урановой смоляной руды (см. уранин), из которых был извлечен весь уран, тем не менее, заметно активны. Они заподозрили, что, кроме урана (и тория), в урановых рудах имеются еще неизвестные нам радиоактивные элементы. В результате очень сложной и длительной переработки тонны отбросов смоляной руды им удалось выделить фракцию, содержащую сернокислый барий, в высокой степени радиоактивную. Из этой фракции, в конце концов, они выделили бромистое соединение нового элемента, по крайней мере, в миллион раз более активного, чем уран; этот новый элемент был назван радием (см.). Из других фракций особо радиоактивной оказалась фракция, содержащая висмут; из нее Кюри выделила не в чистом состоянии и в весьма ничтожном количестве новый элемент — полоний, в тысячу раз более радиоактивный, чем радий. В 1899 г. Дебьерн (Debierne) открыл во фракциях, содержащих редкие земли, в частности лантан, новый радиоактивный элемент — актиний (см.).
Излучение радиоактивных веществ в общем характеризуется прямолинейностью и большой скоростью. Анализ излучения в магнитном и электрическом поле показывает, что оно состоит из троякого рода лучей: α-, β- и γ-лучей. Рис. 1 показывает действие сильного магнитного поля на пучок лучей радия; магнитные линии идут перпендикулярно к плоскости рисунка, северный полюс расположен над рисунком. Очевидно, то α- и β-лучи несут электрические заряды, γ же лучи — нет. Так как направление отклонения указывает на знак заряда, то можно предположить, что β-лучи, несущие отрицательный заряд, аналогичны катодным лучам (см.), а α-лучи, несущие положительный заряд, аналогичны каналовым лучам. Эти лучи представляют потоки наэлектризованных частиц. Так как они испытывают отклонения и в электрическом поле, то измерения величин отклонений в магнитном и электрическом полях дают возможность составить два уравнения с тремя неизвестными: зарядом e, массой m и скоростью v частиц, составляющих данные лучи. Из этих уравнений легко вычисляются скорость частиц и отношение заряда к массе частицы е\m.
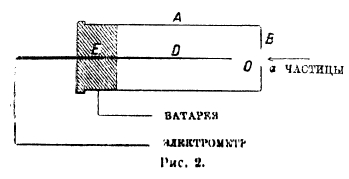
Рис. 2.
α-лучи — это поток положительно заряженных частиц, обычно называемых α-частицами. Если за единицу заряда мы примем заряд одновалентного иона (e = 4,77·10-10 электростатических единиц), за единицу массы — массу водородного атома (m=1,66·10-24г), то отношение e/m у α-частиц оказывается равным ½, следовательно, такая частица или несет один заряд и имеет атомный вес 2, или же несет два заряда и имеет атомный вес 4. Для окончательного решения вопроса надо непосредственно измерить заряд каждой отдельной α-частицы. На рис. 2 показана схема счетчика α-частиц. Через отверстие В в камеру А влетают α-частицы из радиоактивного вещества, находящегося вне камеры; зная величину отверстия В, можно вычислить долю α-частиц, попадающих в камеру от всего числа частиц, излучаемых данным количеством вещества. α-частица, попав в камеру, сильно ионизирует воздух в ней, а так как между металлическим острием Д и оболочкой камеры создается разность потенциалов порядка 5 000 вольт, то ионы, возникшие под влиянием α-частицы, вблизи острия получают большое ускорение и в свою очередь вызывают новую ионизацию воздуха. Таким образом, каждая α-частица, попавшая внутрь камеры, сильно увеличивает электропроводность воздуха в ней, что и отмечается чувствительным электрометром, соединенным с острием Д. Электрометр снабжен зеркальцем, свет от которого падает на фотографическую ленту. Каждое отклонение электрометра вызывает появление зубца на ленте (рис. 3).

Рис. 3.
К той же цели приводит спинтарископ (см.) Крукса (рис. 4). В точке В помещается радиоактивное вещество; выходящие из него α-частицы ударяют об экран С, покрытый сернистым кальцием; каждый удар вызывает вспышку (искру), называемую сцинциляцией. Эти вспышки наблюдаются и подсчитываются через лупу А.

Рис. 4.
Такими способами можно подсчитать, сколько α-частиц испускает в единицу времени определенное количество радиоактивного вещества; с другой стороны, можно определить весь заряд Е положительного электричества α-лучей, испускаемый тем же веществом в единицу времени; разделив Е на число α-частиц, получим заряд каждой частицы: он оказался равным 2. Отсюда следует, что масса α-частицы равна 4, а это есть атомный вес гелия (см.). Следовательно, α-лучи радиоактивного вещества состоят из атомов гелия, несущих два заряда. Это доказано еще следующим образом. Радиоактивное вещество было запаяно в очень тонкостенную стеклянную трубку; последняя была помещена в более широкую и толстостенную трубку, которую после эвакуирования запаивали, α-частицы проходили через тонкие стенки первой трубки, но не второй, и, таким образом, гелий скапливался в пространстве между двумя трубками. Опыт показал, что 1 г радия в одну секунду испускает 3,5·1010 α-частиц и что таким путем в год из 1 г радия образуется 167 мм2 гелия.
α-частицы движутся со скоростью в среднем около 1/10 скорости света и обладают, следовательно, огромной кинетической энергией. При своем движении через данную среду (воздух, металл) α-частицы ионизируют молекулы или атомы среды и теряют свою скорость, расстояние, которое может пройти α-частица, прежде чем потеряет свою энергию, называется дальностью пробега. Эта дальность пропорциональна третьей степени скорости лучей и тем меньше, чем плотнее среда; так, например, α-лучи урана I обладают скоростью 1,40·109 см/сек, дальность их пробега в воздухе при 15° и 1 атм. — 2,67 см, в алюминии — 0,022 мм; скорость α-лучей радия С = 2,06·109 см/сек, дальность их пробега в воздухе 8,62 см, в алюминии 0,065 мм.

Рис. 5.
Путь, по которому движется отдельная α-частица, может быть сделан видимым и может быть сфотографирован. Для этой цели берут сосуд, наполненный воздухом, насыщенным водяными парами; если объем такого сосуда внезапно расширить, то воздух в нем охладится и станет пересыщенным влагой; для того, чтобы образовался туман, необходимы центры концентрации пара (например, пылинки); такими центрами могут быть α-частицы и ионы газа; α-частицы, попадая в такой воздух, ионизируют его на своем пути, и вдоль этого пути образуются линии тумана, которые могут быть сфотографированы (метод Уильсона, рис. 5).
β-лучи, подобно катодным лучам (см.) представляют поток электронов, движущихся со значительною скоростью от 0,8 до 0,998 скорости света. По теории относительности масса движущегося тела тем больше, чем больше его скорость (см. XLI, ч. 7, 420/21); опыт и подсчет показывают, что β-частица в состоянии покоя имеет массу, равную 0,898·10-27 г, или 1/1840-ой части массы атома водорода, если же эта частица движется со скоростью в 1/10 скорости света, то ее масса на 0,5% больше, а при скорости, равной 0,998 скорости света, ее масса в 15,8 раз больше, чем в состоянии покоя. Так как скорость β-частиц больше, а масса меньше, чем α-частиц, то β-лучи способны проходить значительно большие расстояния в материальных средах, чем α-лучи; так, некоторые сорта β-лучей проходят через слой алюминия в 1 см; толщиной алюминиевой пластинки, при прохождении через которую β-лучи теряют половину своей, интенсивности, часто характеризуют сорт этих лучей. Интенсивность же их обычно измеряют по способности ионизировать воздух. Эта способность у β-лучей значительно меньше, чем у α-лучей; так, β-частица со скоростью в 0,9 скорости света образует в воздухе в 200 раз меньше ионов, чем, α-частица.
γ-лучи обладают той же природой, что и рентгеновы лучи (см.): длина волн рентгеновых лучей 1,3·10-7—1·10-9, γ же лучей 1,4·10-8 —5·1011 см (ср. ХLI, ч. 4, 42). Вследствие малой длины волны γ-лучи проникают через материальные среды значительно легче рентгеновых, так как они проходят через слой свинца в несколько см толщиной. Они обладают также и ионизирующей способностью, но (при расчете на единицу пути) значительно меньшей, чем β-лучи.
Лучи радиоактивного вещества производят и химические действия. Так, они превращают желтый фосфор в красный, кислород в озон, вызывают окраску в стеклах, драгоценных камнях, разлагают ряд веществ, в том числе галоидные соединения серебра, чем объясняется их действие на фотографическую пластинку; в водном растворе соли радия непрерывно идет разложение воды с частичным образованием также озона и перекиси водорода; 1 г радия в день образует в растворе 13 см гремучего газа. В газовых системах лучи радиоактивных веществ способны вызывать и синтозы, например, аммиака, воды и др.
Когда лучи радиоактивных веществ поглощаются окружающей средой, их энергия превращается в теплоту; этим объясняется тот замечательный факт, что радиоактивные вещества непрерывно выделяют теплоту; 1 г радия, находящийся в равновесии с продуктами своего распада (см. ниже), выделяет 135—137 кал. в час, из которых на долю потери энергии α-лучами падает 117,7 кал., β-лучами — 12,1 кал., γ-лучами — остальные калории. 1 г чистого радия без продуктов распада выделяет около 25,5 кал. в час.
Характер и интенсивность излучения радиоактивных веществ совершенно не зависят от внешних условий; в наших руках нет средств для того, чтобы заметно изменить течение радиоактивных процессов; при самых низких и высоких температурах, в сильнейших электрических и магнитных полях радиоактивные вещества ведут себя так же, как и в обыкновенных условиях.
Распад радиоактивных веществ. Если соль радия поместить в замкнутый сосуд, то через несколько времени воздух в сосуде становится сильно радиоактивным и остается таковым в течение ряда дней после удаления из сосуда. Резерфорд (см.) показал, что из радия выделяется радиоактивный газ — эманация радия (радон, нитон). Эманация радия обладает всеми свойствами газов: она диффундирует из одного сосуда в другой, сжимается согласно закону Бойля, сжижается при —62°, затвердевает при —71°; химически она инертна и принадлежит к группе аргона. Так как температура затвердевания эманации достаточно высока, то ее можно освободить от газов воздуха и, после превращения в газ, определить ее плотность, а следовательно и атомный вес, что и было сделано Греем и Рамзеем (см.) на особых микровесах; ее атомный вес оказался равным в среднем 223. Плотность эманации в жидком состоянии около 5,5, ее критическая температура 100,5°, критическое давление 62,4 атм. Спектр эманации оказался спектром нового элемента.
Радиоактивность эманации, отделенной от радия, постепенно уменьшается и приблизительно через 4 дня падает до половинного значения; это падение во времени протекает по уравнению:
dl/dt = kl или (в интегральной форме) по уравнению I = I0e-kt гдо I — интенсивность излучения в момент времени t, I0 — та же величина в исходный момент t=o, k — коэффициент пропорциональности, е — основание натуральных логарифмов.
Самым важным фактом оказалось образование гелия из эманации. По мере падения радиоактивности эманации, помещенной в замкнутой трубке, в ней появляется и постепенно накапливается гелий, что было доказано не только спектроскопически, но и непосредственным измерением образовавшегося гелия и определением его физических свойств.
1 г радия дает в секунду 1,24·10-9 см3 эманации, но так как сама эманация непрерывно изменяется, то из 1 г радия получается эманации через 4 дня — 0,311 мм3, а через 30 дней — 0,607 мм3. Это максимальное количество эманации, которое может находиться в равновесии с 1 г радия, получило особое название «кюри».
Если эманации радия пробыла несколько дней в замкнутом сосуде и если остатки ее после этого удалить, то стенки сосуда оказываются радиоактивными. Длительными, сложными и остроумными опытами было доказано, что на стенках имеется смесь твердых радиоактивных веществ, различающихся по своим физическим, химическим и радиоактивным свойствам. Они могут быть разделены различными методами. Можно воспользоваться различием в их летучести (так, радий В улетучивается при 600°, радий А — при 800°-900°, радий С — при 700°-1 300°), различием в их химической природе, благодаря чему они осаждаются из растворов вместе с родственными (обычными) элементами (например, радий родствен барию, полоний — теллуру, радий В — свинцу, радий С — висмуту и т. п.), их различным поведением при электролизе растворов. Такими путями удалось выявить и изучить их свойства. Весьма существенным является их высокая радиоактивность, позволяющая изучать ничтожные их количества, а также часто резкие различия в характере их излучения, что в свою очередь позволяет не только характеризовать эти новые элементы, но и подчас обнаруживать их в смеси с другими.
Теория распада радиоактивных веществ. Все явления радиоактивности получили прекрасное объяснение после того, как Резерфорд дал свою теорию распада радиоактивных веществ. Заслуга этой теории в том, что уже в начале развития учения о радиоактивности она направляла опыт; без нее разобраться в чрезвычайной сложности радиоактивных явлений было бы невозможно. Сущность этой теории состоит в следующем. Радиоактивность есть свойство атома; атомы радиоактивных веществ находятся в неустойчивом состоянии и самопроизвольно разрушаются; распад атомов данного радиоактивного вещества подчиняется статистическому закону, согласно которому количество распадающихся атомов вещества пропорционально всему количеству атомов, имеющихся в наличии в данный момент – dN/dt = kN или в интегральной форме N = N0e-kt, где N0 — число атомов в исходный момент t=0, N — число атомов в данный момент t; так как интенсивность излучения пропорциональна числу распадающихся атомов, то эти уравнения вполне аналогичны приведенным выше.
Уравнение N = N0e-kt показывает, что полный распад вещества наступает (теоретически) через бесконечно большой промежуток времени; в качестве характеристики данного радиоактивного вещества вычисляют время, в течение которого распадается половина имеющихся атомов его:
N/N0 = ½ = e-ktn, откуда tn = ln2/k; это время называется полупериодом распада. Коэффициент k называется радиоактивной постоянной, он показывает вероятность данного атома подвергнуться распаду. Обратная величина 1/k есть средняя продолжительность жизни радиоактивного элемента.
Понятно, что для точной характеристики радиоактивного элемента необходимо иметь его в чистом виде или, в крайнем случае, уметь вычислить его свойства из данных, полученных для смеси их. При достаточно долгом хранении радиоактивное вещество А, распадаясь, образует вещество В, которое, в свою очередь распадаясь, дает вещество С, и т. д. Поскольку образующиеся элементы не летучи, они остаются вместе с материнским элементом, и в результате получается сложная смесь исходного вещества с продуктами распада в состоянии равновесия. Количество радиоактивного элемента в смеси зависит от скорости распада его: чем больше эта скорость, тем меньше его в смеси. Так, например, в минерале на 1 г чистого урана в состоянии равновесия находится 0,000013 мг урана Х1, 0,34 мг радия, 0,0000000011 мг радия А, 0,0032 мг радия D.
По современным взглядам атом состоит из ядра и свиты электронов, движущихся вокруг ядра (см. атом, электрон, и XLI, ч. 4, 70 сл.). Ядро заряжено положительным электричеством; в обычных условиях число внешних электронов равно числу зарядов ядра, и в целом атом является нейтральным. Число внешних электронов, равное числу зарядов ядра, определяет номер (порядковое число) элемента. Ядро состоит из протонов (ядер атомов водорода), α-частиц и электронов. При радиоактивном распаде разрушается ядро атома, из него вылетают или α-частицы, или электроны, образующие тогда β-лучи. Выделение β-частиц из ядра часто сопровождается выделением и γ-лучей. Каждый атом выделяет или одну α-частицу, или одну β-частицу (электрон из ядра). Так как α-частица имеет атомный вес 4, то после ее выделения остается атом нового вещества с атомным весом, меньшим на 4 единицы. Так, атомный вес радия 225,95. После вылета α-частицы остается атом эманации, атомный вес которой должен быть около 222, что и подтверждено непосредственными опытами Грея и Рамзея (см. выше). Так как масса электрона (β-частицы) равна 1/1840 массы атома водорода, то уход одного электрона из ядра заметно не изменяет массы оставшегося атома, но этот уход вызывает перегруппировку составных частей ядра, изменяет заряд его и число внешних электронов, что обусловливает новые химические свойства атома, и в результате получается новый элемент.
Опыт и подсчет показывают, что имеющийся на земле радий практически должен исчезнуть через 10 000 лет. Наличие его в современных минералах наводит на мысль, что он образуется из какого-то элемента. Анализ минералов, содержащих радий, обнаружил в них непременное присутствие урана, причем отношение количеств урана и радия оказалось постоянным. То, что уран является родоначальником радия, было непосредственно доказано Содди: он приготовил раствор тщательно очищенного азотнокислого уранила и через 3 года обнаружил в нем радий.
Тщательными и кропотливыми опытами было доказано существование большого числа радиоактивных элементов, распадающихся на три ряда: 1) ряд урана-радия; 2) ряд актиния; 3) ряд тория. По-видимому, ряд актиния генетически связан с первым рядом, ряд же тория вполне независим. В прилагаемых таблицах показаны в порядке их возникновения все радиоактивные элементы и отмечены главнейшие их характеристики.
Таблица 1
Превращение радиоактивных элементов
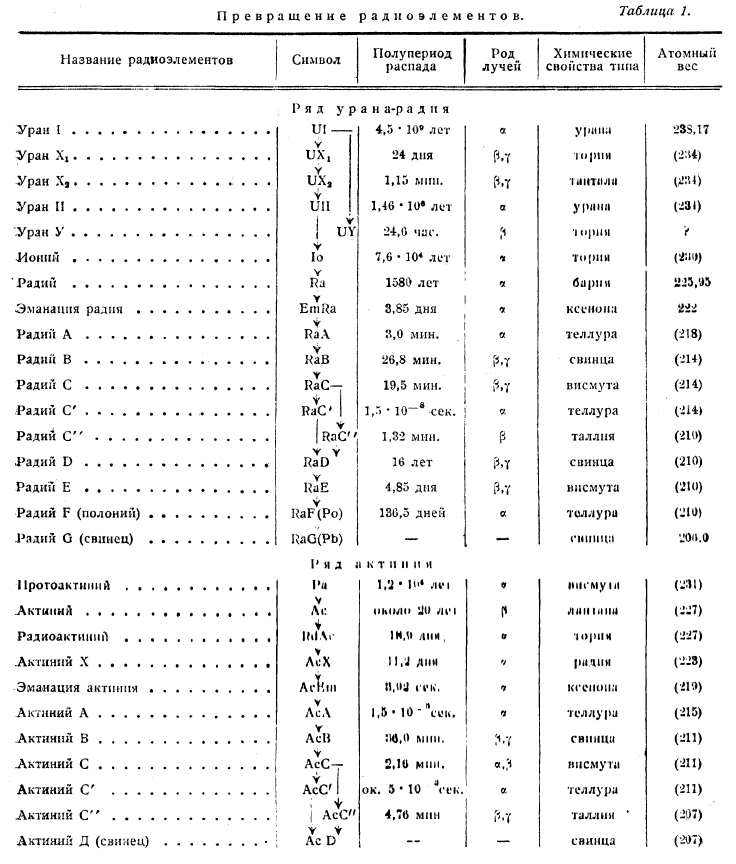

Для ряда радиоактивных элементов, несмотря на ничтожные количества, в которых они могут быть выделены, удалось установить их химическую природу. Сопоставив химические свойства радиоактивных элементов и характер излучения при их возникновении из материнского элемента, Содди и Фаянс установили следующие весьма важные правила:
1) «Элемент, возникший вследствие выделения α-частицы материнским элементом (например, эманация из радия), смещается в периодической системе элементов (см.) на две группы налево»; так, радий находится во II группе, эманация в 0-й (она же VIII гр.), торий в IV гр., мезоторий во II гр. и т. д.
2) «Элемент, возникающий вследствие выделения β-частицы материнским элементом, смещается в ближайшую высшую группу, например, RaD в IV гр., RaE в V гр.».
Эти правила не только позволили выяснить химическую природу некоторых недостаточно изученных радиоактивных элементов, но и привели к установлению новых элементов, а также к открытию совершенно нового явления изотопии элементов. До настоящего времени открыто около 40 радиоактивных элементов с атомными весами между 238 и 206; при размещении их по клеткам периодической таблицы химических элементов, оказалось необходимым помещение в одну и ту же клетку по нескольку элементов. Таблица 2 показывает распределение элементов по клеткам периодической системы от № 81 до № 92.
Таблица 2
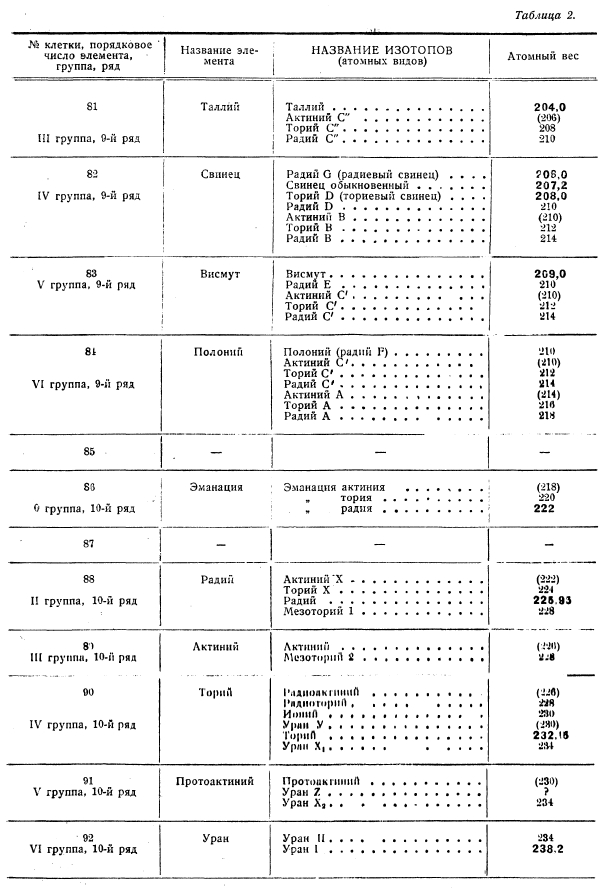
Элементы, находящиеся в одной и той же клетке, получили название изотопов (греческий — «занимающие одно и то же место»). В атомах изотопов ядра имеют один и тот же заряд, количество и орбиты внешних электронов одинаковы, поэтому химические свойства их тождественны, и изотопы химически не могут быть отделены друг от друга. Изотопы могут различаться атомным весом, т. е. строением ядра атома, следовательно, могут различаться по тем своим физическим свойствам, которые являются функциями массы атомов. Например, плотность радиевого свинца 11,273, обыкновенного 11,387.
Явление изотопии, впервые найденное у радиоактивных элементов, оказалось свойственным многим обыкновенным элементам. Астон и Демпстер нашли, что из 53 изученных ими элементов 21 являются чистыми, а остальные — смешанными (т. е. состоящими из смеси изотопов); наибольшее число изотопов найдено у олова, ксенона и ртути (не менее 7). Одна из крупнейших проблем — найти объяснение, почему обыкновенные смешанные элементы, независимо от географического нахождения, геологического возраста и даже космического происхождения (например, земное и метеоритное железо) минералов, в состав которых входят эти элементы, обладают одним и том же атомным весом, т. е. представляют строго постоянную смесь изотопов. Исключение составляют свинцы (см. таблицу 2). Атомный вес свинца, получаемого из нерадиоактивных руд, равен 207,2, атомный же вес свинца из африканской смоляной руды — 206,05, из норвежского торита — 207,90. Эти результаты являются весьма сильным доказательством в пользу теории распада радиоактивных веществ. На самом деле, ряды радия и тория заканчиваются недеятельными свинцами. В ряду превращений от радия до радиевого свинца 5 радиоактивных элементов выделяют α-частицы, т. е. теряют 5х4=20 атомных единиц; а так как атомный вес радия (округленно) 226, то атомный вес радиевого свинца должен быть 226— 20 = 206, что и подтверждено опытом. В ряду от тория до ториевого свинца 6 элементов излучают α-частицы, следовательно, атомный вес ториевого свинца должен быть 232,15—24=208,15. Найденный атомный вес свинца из торита 207,9 весьма близок к этому числу, несколько меньшая величина объясняется примесью урана в торите.
Отметим наиболее важные и интересные из отдельных радиоактивных элементов. Уран представляет смесь изотопов UI и UII, последнего в смеси только 0,04%. Из UII образуется ионий, более долговечный, чем радий, однако выделить его в чистом виде не удалось: он является изотопом тория, и поэтому всегда получается неразделимая смесь тория и иония (все урановые минералы содержат, хотя бы в качестве примеси, торий); получен препарат тория с 30% иония; атомный вес такой смеси — 231,50 (ат. вес Іо—230, Th—232,15). Ионий был открыт Больтвудом в 1907 г.; выделенный им из урановой смоляной обманки торий оказался в 100 000 раз активнее обыкновенного тория и никакими химическими средствами не мог быть очищен. Из UI и UII образуется UZ, дающий боковую ветвь радиоактивных элементов; по-видимому, из UZ образуется протоактиний, родоначальник актиниевого ряда. Это ответвление от U количественно не более 3—4%. Актиниевые элементы всегда присутствуют в урановых минералах. Из ториевых радиоактивных элементов особо важен мезоторий I, изотоп радия. В зависимости от соотношения урана и тория в исходной руде, получаемый из нее радий всегда содержит большую или меньшую неотделимую примесь мезотория. Так как период распада МsTh1 много короче, чем у Ra, то даже из минералов с малым содержанием урана получаются препараты радия с примесью МsTh1, а не обратно. МsTh1 активнее радия в 240 раз, а потому для медицинских целей специально получают радий с возможно большей примесью мезотория I. Необходимо еще отметить поразительное разнообразие в долговечности различных радиоактивных элементов; наряду с у ранами I и II и торием, полупериод распада которых измеряется миллионами и миллиардами лет, имеются радиоэлементы (RaC', ThC'), продолжительность жизни которых измеряется миллиардными долями секунды. К числу радиоактивных элементов надо отнести еще калий и рубидий, излучающие β-лучи. Их активность очень мала, рубидий в 15 раз менее активен, чем уран, а калий в 10 раз менее активен, чем рубидий.
Применение и техническое получение радиоэлементов. Уран и торий находят себе техническое применение независимо от их радиоактивности. Из-за последней медицинское и техническое значение имеют радий, его эманация и мезоторий I. В медицине они широко применяются для лечения рака, болезней кожи и других заболеваний (см. радиотерапия). В значительно меньшем количестве они применяются в производстве светящихся (в темноте) составов, которыми покрывают циферблаты часов, стрелки приборов, рекламные вывески и т. п. В стадии опытов находится применение радия в электротехнике, земледелии и ряде производств.
Главнейшим источником радия является урановая смоляная руда (уранин, см., состоящий в массе из коллоидной окиси урана U3О8) в Бельгийском Конго, затем в Иохимове (Рудные горы Чехословакии) и Корнуэльсе в Англии. В 1926 г. открыты новые богатые месторождения урановых руд в северном Трансваале, в 1927 г. во Франции близ Сен-Реми-сюр-Дюролль, в 1928 г. в Гордонии (Капская провинция). У нас урановая руда добывается из Тюямуюнского месторождения (см. в Ошском кантоне Киргизской АССР, обнаружены, но не разрабатываются, и другие месторождения, как в Киргизской АССР, так и Узбекской ССР и в Восточном Забайкалье. Первое место по добыче радия занимает Бельгия (завод в Оолен), в 1923 г. ею было добыто 48 г радия, что значительно превышает годичную емкость мирового рынка, почему завод временами приостанавливался. В 1927 г. продано было 26 г бельгийского радия. Производство радия в других странах (САСШ, Чехословакии и др.) сильно пало. Всего в мире до 1927 г. получено около 340 г радия, из них 180 г получено было САСШ, потерявшими в 1922 г. свое первенствующее значение в этой области.
Технологическая переработка радиевых руд чрезвычайно сложна и дорога; так как радий весьма родственен и изоморфен с барием, то переработка руд стремится к концентрации бария и радия путем удаления пустой породы, к выделению сырых сульфатов и обогащению их радием; затем сульфаты переводят в хлористые соли, и разделяют соли бария и радия путем длительной и кропотливой фракционированной кристаллизации. Содержание радия в рудах ничтожно. Так, в тонне наиболее богатых руд при 50% урана содержится около 170 мг радия, в бедных рудах это содержание падает ниже 10 мг. Содержание мезотория I в тористых рудах еще меньше, тонна монацитового песка е 5% тория содержит около 6 мг мезотория I. Неудивителен поэтому огромный расход руд и химикалий для получения радия, например 1 г радия из отенита получается из 800 т руды при затрате 300 т химических продуктов, 200 т угля, причем приходится манипулировать с 15 000 т жидкости. Цена радия сильно колебалась: миллиграмм радия-элемента стоил в 1904 г. 400 франков, в 1920 г. — 2 000, в 1923 г. — 1 000 франков, в 1927 г. — 70 долларов.
Радиоактивность и геохимия. Во всех урановых и ториевых минералах содержатся также и продукты их распада, но в ничтожных количествах; так, по Резерфорду, в древних минералах находится иония 3,9·10-4, радия 3,4·10-5, мезотория I 4,2·10-8, эманации радия 5,1·10-10, эманации тория 1,2·10-14, тория А 3,1·10-17 и т. д. С геохимической точки зрения наиболее важным является вопрос о распространении урана и тория в земной коре. Тория больше раз в шесть, чем урана, в среднем их количества доходят до 10-3—10-2 % всей массы земной коры. Главные массы обоих элементов находятся в состоянии крайнего рассеяния во всех породах; в больших количествах они находятся в виде изоморфных примесей или смесей в минералах, содержащих редкие земли и входящих в состав кислых пород и пегматитов тех же пород, в последних они встречаются также в виде урано-ториевых минералов. В базальтовых (основных) породах количества их значительно меньше. Судьбы тория и урана в земной коре сильно разнятся. В результате выветривания гранитовых массивов и уноса текущими водами легких продуктов разрушения образуются россыпи, обогащенные торием; в благоприятных условиях состава гранитов и условий выветривания, особенно при наличии вторичного обогащения россыпей морскими волнами (Бразилия, Индия), образовались монацитовые и ортитовые пески, в настоящее время являющиеся богатейшими источниками тория. Торий резко отличается от урана тем, что его минералы нерастворимы в воде и водой не уносятся, почему все природные воды не содержат или почти не содержат соединений тория. Между тем количество урана, сконцентрированного в пегматитах, составляет только малую долю всего у рана, существовавшего в магме и ушедшего из нее до и после ее затвердения. Растворенные урановые соединения частью осаждаются в конкреционных жилах вместе с другими металлами, часто вдали от гранитного массива, из которого они были извлечены водой, частью попадают в осадочные породы и во все природные воды. Этим свойством урана объясняется то, что урановых минералов значительно больше (около 100), чем ториевых (около 40), и то, что некоторые из них имеют коллоидальную природу (например, иоахимская руда).
Все природные воды радиоактивны, своей радиоактивностью они обязаны почти исключительно урану (и продуктам его распада). Океаны содержат несколько сот миллионов тонн урана, — конечно, в состоянии крайнего разбавления. Уран сообщает радиоактивность также всем источникам и термам, которые выносят его из глубин земли в количествах, по-видимому, превышающих его количество в океанах. Радий, как правило, всегда сопровождает уран, но иногда текущие воды могут их разделить; поэтому попадаются породы, содержащие радий без урана, как, например, некоторые бариты и полиморфиты. Радиоактивность воздуха объясняется присутствием эманации радия в нем, количество ее ничтожно мало —5·10-17%, т. е. в 1 см3 воздуха содержится 1 — 1,3 атома эманации.
Учение о радиоактивности оказало выдающиеся услуги геологии. Укажем на две из них. В результате радиоактивного распада образуется два постоянных элемента: гелий и свинец. Мы знаем скорость образования их из урана; определив опытом в данном минерале, образовавшемся в известную нам геологическую эпоху, содержание урана, радия, гелия и свинца, мы сможем вычислить возраст минералов. Вычисления по гелию дают низший предел возраста, так как гелий, как газ, может улетучиваться из минерала, вычисления же по свинцу вполне надежны. Таким образом, были определены возрасты минералов (по свинцу):
Нижнекембрийской системы – 1500 млн. лет
Среднекембрийской системы – 1300 млн. лет
Верхнекембрийской системы – 1200 млн. лет
Силурийской системы – 450 млн. лет
Девонской системы – 300 млн. лет
Каменноугольной системы – 200 млн. лет.
Эти данные были подтверждены оригинальным методом «плеохроических двориков» в минералах. В некоторых минералах имеются включения очень малых кристалликов циркона. Если к циркону примешан уран или торий, то их α-лучи, проникая в минерал, производят химические превращения и вызывают образования микроскопических плеохроических колец, различающихся в зависимости от природы α-лучей. Эти кольца (дворики) могут быть вызваны искусственно в короткий срок действием сильных препаратов радия, и путем сравнения можно вычислить возраст естественных двориков. Этот метод оказался много чувствительнее электроскопа, с помощью которого можно обнаружить биллионную часть грамма радия, а для того, чтобы около цирконового ядрышка образовался заметный дворик, достаточна миллионная часть биллионной доли грамма радия, количество, которое дает в год только 30 α-частиц.
Распад радиоактивных веществ в конечном результате сопровождается выделением тепла. В год выделяют тепла: 1 г урана — 7 900·10-4, тория — 2 300·10-4, рубидия — 2,38·10-4, калия — 1,24·10-4кал.; грамм изверженной породы дает в год 11,4·10-6кал. Вычисление показывает, что общее количество тепла, выделяемое этими элементами в земной коре, настолько грандиозно, что для объяснения современных термических условий на земле необходимо допустить ограниченное распространение радиоактивных элементов в глубине земли (см. XI, 547); по-видимому, толщина земной коры не больше 16 км. Мы различаем верхнюю оболочку — гранитную, и нижнюю — базальтовую; последняя значительно менее радиоактивна, чем первая. Под океанами базальтовая оболочка подходит довольно близко ко дну их, в области материков гранитная оболочка имеет 8—16 км толщины. Гранитные массивы плавают в базальтовом ложе, как льдины в воде. Расчеты Джоли и Гольмса показывают, что благодаря радиоактивных веществ в течение геологического времени (около 1010 лет) наша земля не нагревается и не охлаждается, периодически только накопившееся в глубине коры тепло дает повод к усиленной геологической деятельности: под влиянием повышенной температуры базальтовое ложе делается менее плотным, материки погружаются в него глубже, наступают горообразовательные и вулканические процессы, трансгрессии моря.
Не только геология, но и космогония черпает из учения о радиоактивности новые идеи. Одним из капитальнейших является вопрос об односторонности радиоактивных процессов. Если радиоактивные вещества только разрушаются, то почему они в бесконечном времени существования вселенной не исчезли совсем? Необходимо допустить их образование во вселенной (Нернст). Конечным продуктом распада урана и тория является не радиоактивный свинец. Не являются ли другие не радиоактивные элементы конечными этапами распада радиоактивных элементов, более тяжелых, чем уран, и ныне уже исчезнувших? Новейшие исследования «космических лучей» показывают, что элементы, по крайней мере гелий, кислород, кремний и, по-видимому, железо, в глубинах вселенной образуются непосредственно из протонов и электронов. Очевидно, что гипотеза о происхождении обыкновенных элементов из радиоактивных не обязательна и во всяком случае не всеобъемлюща, но несомненно, что некоторые элементы во вселенной возникают, а следовательно, могут рождаться и радиоактивные элементы.
Литература: М. S. Curie, «Recherches sur les substances radioactives», Paris, 1903 (есть русский перевод А. И. Бачинского); F. Soddy, «The Chemistry of the Radioelements», 1914—15 (есть русский перевод); Е. Rutherford, «Radioactive Transformations», London, 1906; М. S. Curie, «Тгаіté de radioactivité», Paris, 2 т. 1-е изд. 1910 (немецкий перевод «Die Radioactivität», 2 т. 1912); Е. Rutherford, «Radioactive Substances and their Radiations», Cambridge, 1913 (немецкий перевод «Radioactive Substanzen und ihre Strahlungen»); А. Debierne, «Recherches sur les phénomènes de radioactivité», Paris, 1914; «Handbuch der Radiologie», herausgegeben von Е. Marx, Leipzig, 5 т.; F. Нenrich, «Chemie und chemische Technologie radioaktiver Stoffe», Berlin, 1918; Maurice Curie, «Le Radium et les Radio-Еléments», Paris, 1915; K. Fajans, «Radioaktivität und die neuste Entwicklung der Lehre von den chemischen Elementen», Braunschweig, 1921 (есть русский перевод); G. v. Hevesy, F. Paneth, «Lehrbuch der Radioaktivitat», Leipzig, 1923 (есть русский перевод); St. Meyer und Е. Schweidler, «Radioaktivität», 2 изд. 1927; статьи по радиоактивности в «Основах химии» Д. И. Менделеева, 9-е изд., II т., 1928.
А. Раковский.
| Номер тома | 35 |
| Номер (-а) страницы | 331 |
