Серная кислота (производство и применение)
Серная кислота (производство и применение). Для добывания серы кислота в технике применяются два способа: камерный и контактный. Оба способа практически и теоретически очень хорошо разработаны, так что со стороны выходов серной кислоты тот и другой не оставляют желать большего.
1. Камерный способ. В основу его положена реакция окисления сернистого газа (SO2) кислородом воздуха в серной кислоте в присутствии паров воды и окислов азота по равенству: SO2 + Н2О + О = H2SO4.
Эта основная реакция протекает в свинцовых камерах, почему и способ носит название камерного. Окислы азота играют роль катализатора (или ускорителя реакции) и в окончательном продукте не содержатся. Ускоряющая роль их основывается на свойстве окиси азота быстро окисляться насчет кислорода воздуха в двуокись азота: NО + О = NO2; двуокись же азота в присутствии воды, в виде паров и сгустившегося тумана, превращается в азотную и азотистую кислоту: 2NO2 + H2O = HNO3 + HNO2.
Азотная кислота является окислителем сернистого газа, раскисляясь до азотистой: HNO3 + SO2 = HNO2 + SO2; SO2 + H2O = H2SO4. Что же касается до азотистой кислоты, то ее роль сводится к следующему: растворенная HNO2 в воде распадается на азотную кислоту, окись азота и воду: 3HNO2 ↔ HNO3 + 2NO + H2O; но этот распад сам по себе никогда не доходит до конца; в присутствия же SO2 распад ускоряется: азотная кислота окисляет сернистую кислоту, раскисляясь до HNO2 окись же азота, выходящая из круга действия в окружающую воздушную атмосферу, снова окисляется в двуокись азота, и таким образом круговорот превращений начинается снова. Изучение процесса окисления SO2 в присутствии окислов азота со стороны кинетики его (протекания во времени), на основании опытов Трауца, дало автору этой статьи возможность объяснить весь процесс по указанной схеме (Е. Я. Орлов, «Исследования в области кинетики химических реакций и катализа», стр. 207—213). Сернистый газ, необходимый для превращения в серную кислоту, получается сжиганием серы или сернистых металлов (например, FeS2, ZnS) в особого устройства печах насчет кислорода воздуха, поступающего в печи из воздушной атмосферы; одновременно с кислородом, который требуется для образования SO2, при посредстве тех же печей доставляется в камеры и избыток его, нужный для дальнейшего окисления SO2 в H2SO4. Так как вещества, вступающие в реакцию, находятся в газообразном (например, SO2, O2) или парообразном (H2O) состоянии и притом в громадных количествах и, кроме того, так как для доведения процесса до конца требуется время, то становится понятным, почему для помещения реагирующих веществ необходимы большие замкнутые пространства, где эти вещества остаются некоторое время и вступают между собой в реакцию, в результате которой из газообразного SO2 образуется жидкая H2SO4, скопляющаяся на дне вышеупомянутых помещений. Если бы мы подсчитали, сколько воздуха потребуется лишь теоретически для сжигания серы (или железного колчедана, цинковой обманки) в SO2 и дальнейшего окисления его в SO3 на основании равенств:
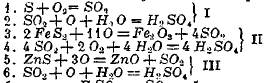
то для образования H2SO4 из SO2, добываемого сжиганием 1 кг серы в форме сырой серы, железного колчедана и цинковой обманки, — нам необходимо было бы ввести в печь: 5 211,6 247 и 6 666 литров воздуха при 0° и 760 мм барометрического давления. Таковы строго теоретические количества воздуха, вводимого в печь для нужных превращений. Но практика установила, что для успешности окисления SO2 необходим некоторый избыток кислорода сравнительно с теоретическим количеством его, так чтобы в исходящих газах этот избыток кислорода равнялся 5—8%, при сжигании S, и 6,4—8%, при сжигании FeS2 или ZnS; на основании этого для сжигания 1 кг серы расходуется воздуха значительно больше теоретического количества.
Не вдаваясь в подробности вычислений, ограничимся здесь лишь приведением цифр: количеств потребного для процесса воздуха, количеств образовавшихся печных газов и состава их, в предположении, что в отходящих из камер газах содержится 8% кислорода и 92% азота (интенсивный ход процесса):
|
1 кг серы, сгоревшей в форме: |
Сырой серы (100%) |
Колчедана (с 50% S) |
Цинковой обманки |
|
I. Потребует атмосферного воздуха в литрах (при 0° и 760 мм рт. ст. давления). |
7918 |
9237 |
9853 |
|
II. Получается печных газов в литрах (при 0° и 760 мм). |
7918 |
8976 |
9505 |
|
III. Состав печных газов SO2 в объемных %% |
9,42 |
7,75 |
7,32 |
|
О2 в объемных процентах |
11,58 |
10,95 |
10,78 |
|
N2 в объемных процентах |
79 |
81,30 |
81,90 |
|
IV. Отношение I к II |
100 |
97,2 |
96,5 |
|
V. Отходящих газов в литрах при 0° и 760 мм давления |
6799 |
7932 |
8461 |
Из этой таблицы мы убеждаемся, что объемы печных газов, полученных из трех сырых материалов, относятся как 7,918:8 976:9 505 = 1:1,133:1,2. Предположим, что в сутки мы сжигаем200 пуд. серы, или 3 200 кг; следовательно, в 1 мин. 2,22 кг. Тогда количества печных газов, поступающих в камерную систему в 1 мин. при сжигании серы в форме серы, колчедана (с 50%S) и цинковой обманки, равняются: 15,89; 19,93 и 21,1 куб. м. Если принять во внимание, что в гловеровой башне, при современном устройстве камерной системы, окисляется около 20% всего сернистого газа, а остальные 80% окисляются в камерах, тогда в камеры войдут количества газов: 15,89 х 0,972 = 15,4 куб. м (в случае горения сырой серы); 19,93 х 0,977 = 19,47 куб. м (в случае 50%-го колчедана) и 21,1 х 0,978 = 20,64 куб. м. (в случае ZnS). При средней же температуре обращающихся в камерах газов в 40°С, эти количества надо увеличить на температурный коэффициент (273 + 40)/273 = 1,146; отсюда количества газов, поступающих в камеры в 1 мин.: 17,65; 22,3; 23,65 куб. м. При устройстве современных камер считается достаточным 1 куб. м камерного пространства на 1 кг сжигаемой серы в сутки. Следовательно, при сжигании 3 200 кг серы, камерное пространство принимается в 3 200 куб. м Отсюда в 1 мин. должно использоваться 3200/1146 = 2,22 куб. м камерного пространства. Отношения 17,85 к 2,22 = 8; 22,3 к 2,22 = 10 и 23,65 к 2,22 = 10,6. Числа 8; 10; 10,6 — коэффициенты средней технической утилизации камерного пространства. Если мы располагаем 3-х камерной системой для производства H2SO4, то, на основании исследования Г. Люнге, в 1-ой камере производится около 75% всей серной кислоты, во 2-ой кислота — 20% и в 3-ей кислота — остальное; отсюда коэффициент утилизации 8 (в случае сжигания серы) надо увеличить, а именно: для 1-ой камеры 8 умножить на 3 и 0,75, получим 18; для 2 камеры 4,8 и третьей камеры 1,2. Чем выше коэффициент средней технической утилизации, тем с большей выгодой используется камерное пространство в одно и то же время, тем интенсивнее работа камер. Интенсивность работы камерной системы зависит: 1) от количества вводимого в печи воздуха (правильности тяги); 2) от количества вводимых в камеры окислов азота и 3) наконец, от целесообразного устройства камер. Количество вводимого в печи воздуха или правильность тяги контролируется анализом как печных (поступающих в камерную систему, пред гловером), так и отработавших (в конце камерной системы, за Гей-Люссаком) газов: на содержание SО2 в печных газах в случае сжигания
|
|
Сырой серы |
Колчедана (с 50% S) |
Цинковой обманки |
|
Вялый ход, % |
11,2 |
8,59 |
8,1 |
|
Быстрый ход, % |
9,4 |
7,75 |
7,3 |
|
На содержание кислорода в исходящих газах: |
|||
|
Вялый ход, % |
5 |
6,4 |
6,4 |
|
Быстрый ход, % |
8 |
8 |
8 |
Для правильности тяги, при герметичности труб и камер, так чтобы не было засасывания лишнего воздуха, кроме упорядочивания ее при помощи отверстий в дверках печей или поддувальных помещений, заслонок за печами и позади Гей-Люссаковой башни, важно располагать уровень печей (колосниковых решеток) относительно дна камер так, чтобы дно последних отстояло от пода печи на 7—7,5 м. В современных устройствах это требование необязательно; для усиления тяги ставится между гловером и камерами эксгаустор (вентилятор). Чем больше окислов азота обращается в камерах, тем интенсивнее протекает процесс образования серной кислоты. Если перечислить окислы азота на исходный материал — расходуемую чилийскую селитру, то минимум интенсивности достигается при 10% расходуемой селитры по весу сжигаемой серы, а максимум при 15—16%. На утечку и плохое улавливание окислов азота приходится 2,25—3,5% по весу серы, остальное количество, до 10 или 15—16%, должно обращаться в камерной системе, совершая круговорот превращений. Целесообразным устройством аппаратов, действующих в камерной системе, стремятся достичь наилучшего перемешивания обращающихся в системе газов; для этого строят всегда не одну камеру, а несколько (чаще всего 3), ставят между ними реакционные башни (вроде полочной башни Люнге), вместо камер прямоугольного сечения — строят их круглого сечения, с тангенциальным впуском газов вверху и выпуском внизу каждой камеры (система Т. Мейера). При наличности в камерной системе гловеровой и гейлюссаковой башен надлежащих размеров, когда между камерами поставлены реакционные башни, признается достаточным 1 куб. м камерного пространства на 1 кг сжигаемой серы; при устройстве же камер круглого сечения с тангенциальным впуском газов вверху каждой камеры (по Т. Мейеру), считается достаточным 0,5 куб. м на 1 кг сжигаемой серы. В современных же новых устройствах между камерами ставятся особые волчки, помогающие разбрызгиванию нитрозы, азотной кислоты с газообразными продуктами, обращающимися в камерном пространстве. Этим достигается более интенсивное перемешивание реагирующих веществ, ускорение реакций и уменьшение камерного пространства через это. Последнее весьма важно ввиду сокращения основного капитала на постройку и увеличения выходов с кв. м камерной площади или с куб. м того же пространства. В камерной системе не должно быть больше 3 камер. Об интенсивности камерного процесса можно судить и по температурам, которых следует держаться в различных камерах для правильности процесса. Следующая таблица дает средние результаты 10 наблюдений, при средней внешней температуре в 18° (в 3-х камерной системе).
Труба, идущая от гловеровой башни - 73°
Передняя стенка 1-й камеры – 69°
Средина продольной стенки в 25 см от стенки, внизу – 70°
- в середине – 72°
- вверху – 76°
вторая камера – 50°
третья - 29°
Правильность работы камер зависит также от количества вводимого в камерную систему пара (воды). Количество последнего, в виде ли пара или в виде воды, приведенной в мелко раздробленное состояние, контролируется крепостью получающейся на дне камер кислоты.
В случае 3-х камерной системы крепость серной кислоты в градусах Боме:
|
|
Капельная кислота на стенках |
Кислота на дне |
|
В 1-й камере (1 половина; 2 половина), ° |
51-54 |
54-55 |
|
Во 2-й камере, ° |
45-47 |
48-48,5 |
|
В 3-й камере, ° |
45-50 |
48-48,5 |
Для получения H2SO4 удельного веса 1,615 (=70%) или в 55°, на 1 кг сжигаемой серы требуется воды:
1) Для получения H2SO4 98/32 моногидрата (H2SO4)
18/32, или 0,5625 кг
2) для разбавления до 1,615 удельного веса
30.98/70.32, или 1,3125 кг
Итого: 1,875 кг.
Из этого количества воды надо выбросить то количество ее, которое доставляется гловерной башней при ее работе на упаривание от крепости 1,615 до крепости 1,73 (80%)
10.98/70.32, или 0,4375 кг
Остается 1,4375 кг.
Итак, на 1 кг сжигаемой серы надо в камеры вводить 1,4375 кг воды в виде пара или в мелко раздробленном состоянии.
На производство пара, упаривание серной кислоты от крепости 50—53° Б. до крепости в 66°Б., а также на механическую работу поднятия кислоты (при помощи сжатого воздуха) требуется топливо; количество его по Сорелю определяется так: для получения 100 кг серной кислоты в 50—53°Б. расходуется 3,85 кг угля; или сгущения этой кислоты и получения 100 кг ее в 93 % расходуется 18,06 кг угля. Таким образом, общий расход угля определяется в 27,9—28% по весу получаемой 93%-ной кислоты. По другим данным несколько меньше.
В состав камерной системы входят следующие аппараты:
1) Печи для сжигания серы, сернистых металлов (колчеданов, цинковой обманки); они одновременно служат и для введения кислорода воздуха (вместе с азотом последнего) в камеры.
2) Приспособления, устраиваемые при печах или отдельно, для улавливания пыли, уносимой газами из печей.
3) Прибор для введения азотной кислоты (нитрозы) и преобразования ее в окислы азота; таким прибором служит обыкновенно башня Гловера, или просто гловер.
4) Свинцовые камеры, в которых происходят окисление сернистого газа и серной кислоты; последняя, крепостью 50—53°, собирается на дне камер (наивысшая крепость, допускаемая в камерном производстве: 50—53° Б.).
5) Аппарат для улавливания отработавших окислов азота. Таким аппаратом служит башня Гей-Люссака (гей-люссак).
6) Свинцовые чрены для упаривания камерной серной кислоты от крепости 50—53° до крепости 60—62°Б.
7) Аппараты для упаривания серной кислоты от 60—62°Б. до 66°Б.
8) Аппараты для усиления интенсивности реакций, вроде башни Люнге, тангенциального впуска газов в круглые камеры, волчков для распиливания нитрозы с камерной кислотой и смешивания с газами.

Рис. 1 изображает завод для добывания камерной кислоты в 50—53°Б. в схематическом виде. 1. .1 колчеданные печи, в которых происходит сжигание колчеданов (пиритов). Образующиеся печные газы (состав их см. выше) поступают в общий боров над печами (16) и из него при помощи чугунной трубы (2 ) входят в гловерову башню (гловер; на рис. обозначен 3); гловерова башня спаивается из толстых свинцовых листов со свинцовым дном, представляющим таз, и свинцовой крышкой, служащей для распределения кислоты (камерной и нитрозной); изнутри по стенкам она выложена кислотоупорными кирпичами; внутренность ее заполнена кислотоупорным материалом; камерная и нитрозная кислота из сборного бака (19) поступает на крышку башни, распределяется на ней и чрез особые отверстия, закрываемые свинцовыми колпачками, заливается в башню, стекает по кислотоупорному материалу вниз; навстречу кислоте поднимаются печные газы из трубы (2); газы денитруют нитрозу, т. е. раскисляют ее до окиси азота; в то же время своей теплотой уваривают ту кислоту, которая стекает им навстречу; уваренная кислота, до крепости в 62—60° Б., вытекает из гловера и поступает по свинцовой трубе в холодильник (13), где она охлаждается до комнатной температуры и собирается в свинцовый ящик (12) для расходования. Отработавшие печные газы температуры 70—80°С из гловера поступают по свинцовой трубе (4) в свинцовые камеры (5, 6 и 7); здесь происходит главная реакция превращения сернистой кислоты и серной кислоты крепостью в 50—53° (в первой камере) и несколько слабее (во 2-й и 3-й камерах); свинцовые камеры представляют собою комнаты, сделанные из свинца; стенки их на свинцовых лоскутках подвешиваются к деревянным стойкам и балкам фонаря, который служит каркасом для камер; свинцовая крышка припаивается по сторонам к стенкам камер и для избегания прогиба подвешивается при помощи свинцовых лоскутков к верхним балкам фонаря; через крышу камер подается внутрь пар по трубам (21); дно камер не припаивается к стенкам, а образует таз; дно также делается из свинцовых листов; на дне собирается камерная кислота; чтобы газы, обращающиеся в камерах, не проникали наружу, нижние края стенок камер опущены в жидкость, скопляющуюся на дне, и таким образом для газов получается гидравлический запор. Отработавшие в камерах газы, — состоящие из атмосферного азота, избытка кислорода (5—8 объемных %) и окислов азота, — по трубе (18) проходят в две гей-люссаковы башни (8 и 10): последние, подобно гловеровой, также делаются из свинцовых листов, подвешиваются для прочности в деревянных решетованиях (фонарях); внутри они заполняются или кислотоупорным материалом, или коксом (на рис. коксом); отработавшие газы вступают в низ башни и поднимаются вверх; навстречу им по коксу стекает серная кислота в 60—62° Б., которая получается в гловеровой башне; отработавшие газы, увлекающие с собою ценные окислы азота при своем прохождении вверх, отдают в присутствии кислорода окислы азота серной кислоты; последняя стекает на дно башен крепостью на 0,5°Б. слабее первоначальной кислоты, но зато с содержанием окислов азота; эта кислота носит название нитрозы; из гей-люссаковых башен газы, состоящие из одного азота и избытка кислорода, по трубе (11) отводятся в вытяжную трубу, откуда выпускаются в атмосферу. Отекающая из гей-люссаковых башен нитроза (или нитрозная кислота) собирается в баки (12), откуда перепускается в чугунный, выложенный свинцом котел, называемый кислотоподъемником (монтжю) (15); кислота из этого котла сжатым воздухом подается наверх гловеровой башни, в бак (19), откуда она перетекает на крышку последней и с нее внутрь самой башни на кислотоупорный материал. Гловерова кислота из сборника (12) перепускается в чугунный, выложенный свинцом котел, кислотоподъемник (14); из него сжатым воздухом кислота поднимается наверх гей-люссаковых башен — в бак, выложенный свинцом (20); из него стекает на крышку башен и внутрь их, на кокс. Свинцовые камеры, для наблюдения за температурой и крепостью образующейся в них серной кислоты, снабжены по стенкам термометрами и кислотными столиками: на последних стоят цилиндры с опущенными в них ареометрами Боме; стекающая по стенкам кислота попадает в цилиндр, заполняет его; ареометр, плавающий в кислоте, показывает градусы крепости. 2-я и 3-я камеры снабжаются также фонарями (окнами) для наблюдения за цветом камер: цвет газов во 2-й камере должен быть желтым; в 3-й камере — бурым. Такие же фонари устраиваются в соединительных трубах между гей-люссаковыми башнями и в трубе за последним гей-люссаком. Газы, выходящие из гей-люссака, не должны быть окрашены в желтый цвет. В канале, отводящем печные газы из колчеданных печей, иногда ставят чугунные горшки (или корыта, 17 на рис.); в них засыпают селитру, и через воронку заливают кислоту; последняя действует на селитру; выделяющаяся азотная кислота уносится с печными газами в гловер. О количестве расходуемой селитры на 100 весовых частей серы см. выше. Такова схема камерного производства.

Рис. 2
Рис. 2 изображает серную печь в продольном разрезе и рис. 3 — ту же парную серную печь спереди ив поперечном разрезе: на поду, представляющем чугунный лоток (а), сжигается сера; печные газы чрез отверстие f поднимаются в верхнюю часть печи, проходят обратный путь к каналу i, из него в сборный боров k. Сера на лоток забрасывается спереди в отверстие; для этого дверка приподнимается при помощи блока. Верхняя часть печи предназначается для лучшего перемешивания возгнанных паров серы с воздухом и окончательного сгорания их; g — дверка, служащая для установки на решетку горшков селитры с серной кислоты; h — отверстие, обыкновенно закрываемое, для наблюдения за горением серы в верхней половине печи. Подобного типа печей для каждой камерной системы устраивается несколько, например, 6, 8, 12.

Рис. 3
Рис. 4 и 5 изображают колчеданную (пиритную) печь для сжигания крупных кусков колчедана: на колосниковую решетку чрез рабочее отверстие а забрасывается колчедан (пирит) в крупных кусках; слой его немного не доходит до рабочего отверстия; дверка е служит для переворачивания колчедана во время его горения; дверка с ведет к колосникам для повертывания их, когда требуется удалить колчеданные огарки с решетки; d — дверь, ведущая в поддувало или зольник; через ряд отверстий в ней поступает нужный для горения колчедана воздух. Над печами, во всю их ширину, устраивается сборный канал для печных газов; в нем также осаждается увлекаемая из печей пыль. Рис. 6 изображает подвижные чугунные колосники для этой печи (А и В) и ключ для отвертывания их (С). Такие колчеданные печи для сжигания кускового пирита теперь вышли из употребления. Для сжигания колчеданной мелочи служат печи Малетра. я Герресгофа.

Рис. 4.
Рис. 5.
Рис. 7 и 8 представляют полочную печь Малетра (рис. 7 — продольный; рис. 8 — поперечный разрез парной печи): на полках из кислотоупорного материала с, d, е, f, g засыпается слоем колчеданный порошок и сжигается; печные газы удаляются чрез отверстие m в общий канал над печами n, а из него в отводную трубу о. Воздух, необходимый для горения серного колчедана, подается в поддувало по трубке I. Над печами расположены упарные коробки r (для упаривания серной кислоты).
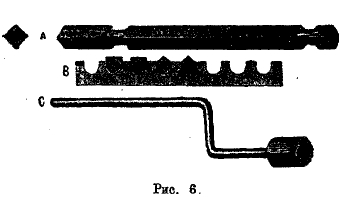
Рис. 6.
Механическая печь Герресгофа, изобретенная в 90-х годах прошлого столетия, в замену печей Малетра, постепенно вытеснила печи других изобретателей и, особенно, печи, требующие ручной работы. В печи Герринсгофа, имеющей обычно диаметр 3,5 м и высоту цилиндрической части также 3,5 м, в течение суток можно сжечь до 3-х тонн серного колчедана, содержащего 45—50% S. Расход силы на вращение вала печи не превышает ½ л. с. Наблюдение за такими печами несложно, и за границей есть заводы, где за 20—30-ю печами наблюдает один рабочий. Печь Герресгофа (рис. 9) представляет вертикальный железный цилиндр А, выложенный изнутри огнеупорным кирпичом. Печь имеет 6 сферических, сделанных из огнеупорных кирпичей сводов Е, Е1, Е2, Е3, Е4 и Е5 образующих пять камер I, II, III, IV и V. В центре печи помещается вращающийся вертикальный полый чугунный вал с карманами, в которые вставляются гребки, (руки) K1, K2, K3 и т. д. Эти гребки снабжены зубьями, расположенными под углом в 45° (рис. 10). При движении такого гребка по часовой стрелке, колчедан, находящийся на сводах, будет передвигаться от центра печи к периферии. При направлении зубьев, гребка в другую сторону, при том же направлении движения гребка, последний будет передвигать колчедан от периферии печи к ее центру. Колчедан в виде мелочи (кусочки около 2—6 мм) загружается в карман В, откуда гребком (2) с зубьями (3) передвигается к валу печи. Передвигаемый по этому верхнему своду Е колчедан не горит, ибо этот свод не находится в замкнутом пространстве; здесь колчедан только подсушивается и поступает через кольцевое отверстие о—о на первый рабочий свод Е, в камеру J, где происходит горение и где колчедан движущимися гребками К1—К2 передвигается к периферии. Чрез ряд отверстий М, находящихся на первом рабочем своде Е1 колчеданная мелочь проваливается в камеру II на второй рабочий свод Е2, где гребками передвигается к валу. Вблизи вала имеются отверстия L—L, через которые колчедан проваливается на свод Е3, где передвигается гребками от центра печи к периферии, и т. д. С нижнего свода Е1 колчедан в виде огарка, состоящего из окиси железа с небольшим остатком несгоревшей серы (1—1,5%), проваливается в отверстие на периферии и собирается в вагонетку. Необходимый для процесса горения колчедана воздух поступает в печь чрез отверстия (5), находящиеся в камере V. Газы движутся в направлении, обратном движению колчедана: именно, из нижней камеры V они поступают чрез кольцевое отверстие L1, в своде Е4 в камеру IV, откуда через ряд каналов (4), находящихся в футеровке печи, поступают в камеру III. Из камеры III газы чрез кольцевое отверстие L1 находящееся в своде Е2 поступают в камеру II и т. д. Из І-й камеры газы выходят через канал Н в сборную трубу. Температура в печи, в особенности во IІ-й камере, достигает 650—680°C. С нижней же полки (Е5) колчеданный огарок выходит уже достаточно остывшим. Через полый чугунный вал, который вращается, вследствие естественной тяги протягивается воздух, который и охлаждает стенки вала и предохраняет его от коробления.
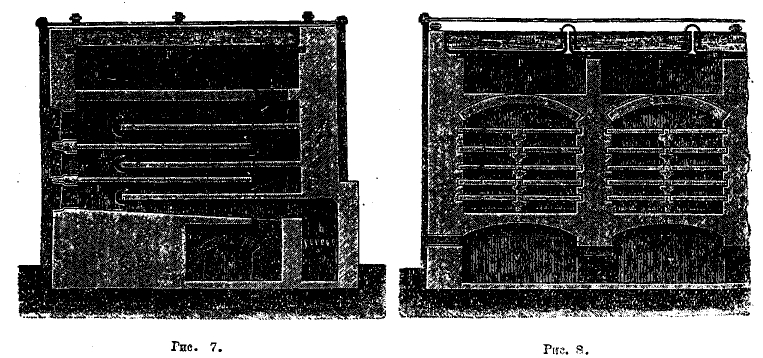
Рис. 7. Рис. 8
Тис. 11 изображает расположение и устройство аппаратов для упаривания серной кислоты от 60 до 66°Б. Серная кислота в 60°Б. поступает самотеком в платиновую чашку аппарата а; дно этой чашки прогревается непосредственно пламенными газами, отходящими из топки; кислота на дне упаривается до 66° Б. и вытекает по трубке k и платиновому колену I в сборный стакан, в котором кислота охлаждается водой, циркулирующей по змеевику; из сборного стакана по сифонной трубке она поступает в стакан m, а из него в бутыль. Пары разбавленной серной кислоты по трубе d отводятся в общий сборник e, охлаждаемый водою; собирающаяся серная кислота незначительной концентрации отводится воронкой и трубкой g в особый сборник. Трубки і и h предназначены для притока холодной воды, служащей для охлаждения стенок свинцовой части аппарата b со шлемом. Эти аппараты, вследствие дороговизны платины, теперь вышли из употребления.
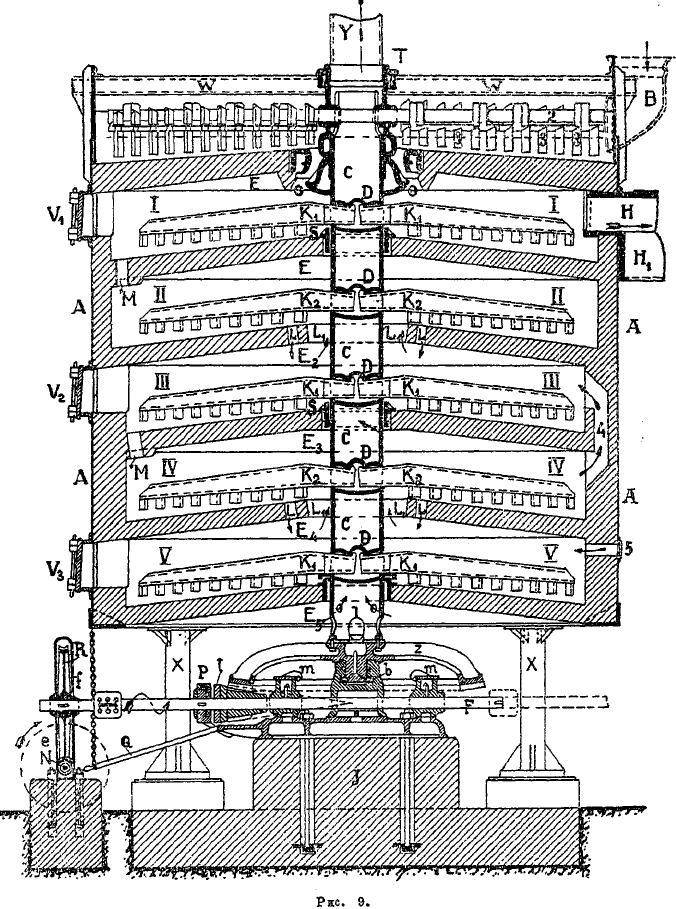
Рис. 9.
Одним из употребительных и совершенных аппаратов для концентрации серной кислоты в настоящее время является аппарат Кесслера. На рис. 12 изображен продольный его разрез, а на рис. 13 — поперечный. Самый аппарат состоит из рекуператора А и сатуратора В. Весь аппарат собирается из кислотоупорного материала, каковым является застывшая лава, залежи которой находятся во Франции (Вольвик) и да Кавказе (близ Владикавказа). По своему химическому составу лава есть не что иное, как застывшее непрозрачное (вследствие медленности охлаждения) стекло. Аппарат составлен из лавовых отдельных частей, снаружи опаянных толстым свинцом. Камерная серной кислоты, предназначенная для концентрации (упаривания), поступает в отверстие С, находящееся в крышке рекуператора А. Последний представляет собой колонну, в сечении квадратную, с 6 (5) горизонтальными полками Р....Р. Полки — толстые плиты из лавы с овальными отверстиями, перекрытыми фарфоровыми колпачками с зазубренными нижними краями. Чрез эти перекрытые колпачками отверстия проходят горячие продукты горения генераторного газа или нефти. Кислота, поступившая на верхнюю полку рекуператора А, стекает на нижележащую чрез особые отверстия (по одному) на полке, исключая последнюю, на которой всегда находится некоторый, небольшой высоты, слой серной кислоты; через нее у колпачков пробулькивает горячий газ. С самой нижней полки рекуператора кислота поступает в сатуратор В, разделенный поперечными вертикальными перегородками S (из лавы), не доходящими до дна ее. Кислота держится на несколько миллиметров выше этих перегородок. Горячие продукты горения (из генератора или же из нефтяной топки), имея температуру в 600—650°С поступают в канал D и проходят над слоем кислоты, а у перегородок S — чрез слой ее. Далее, продукты горения поступают в рекуператор А, где проходят через отверстия с колпачками. Концентрированная горячая серная кислота (купоросное масло) стекает через сосок в холодильник, откуда поступает в сборники для хранения и последующей разливки в стеклянные бутыли, железные бочки или же цистерны. В аппарате Кесслера горячие продукты горения непосредственно соприкасаются с концентрируемой серной кислотой, причем движение продуктов горения и серной кислоты, подлежащей концентрации, происходит по принципу противотока: слабая серная кислота встречает наименее горячие продукты горения в рекуператоре, и, наоборот — горячие продукты горения в сатураторе встречают на своем пути достаточно концентрированную серную кислоту. Из рекуператора (А) отработанные продукты горения вместе с парами воды, выделяющейся из серной кислоты при ее концентрации, а также с увлекаемыми частицами Н2SО4, SO3 и SO2 уходят в трубу R, а затем в конденсатор для улавливания серной кислоты с парами воды. Конденсатор есть не что иное, как деревянный спаянный свинцом изнутри ящик, наполненный коксом; благодаря большой поверхности кусков последнего, конденсируемые пары воды и серной кислоты удерживаются в ящике отработавшие же продукты горения поступают в вентилятор, а из последнего в дымовую трубу. В аппарате Кесслера для приведения в движение продуктов горения и направления их по всей системе всегда пред дымовой трубой ставится вентилятор. Кроме того, пред самым аппаратом имеется полугенератор для сжигания кокса или антрацита для получения продуктов горения, необходимых для упаривания кислоты, или вместо полугенератора можно пользоваться нефтяной топкой. Так как очень важно, чтобы продукты горения не содержали копоти (сажи), то в канале, соединяющем полугенератор или нефтяную топку с аппаратом Кесслера, имеется ряд отверстий, через которые впускается дополнительный воздух для сгорания того, что не успело сгореть в полугенераторе или в нефтяной топке. В качестве топлива рекомендуется кокс, антрацит (но не дрова, торф, каменный уголь) или нефть. Расход топлива составляет около 10—11% от веса получаемого купоросного масла.
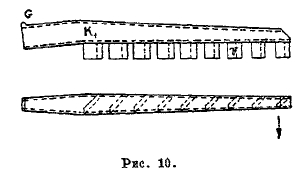
Рис. 10.
Кроме аппарата Кесслера, для концентрации серной кислоты рекомендуется аппарат Гайяра (Gaillard), по принципу работы одинаковый с первым. В этом аппарате в верхней части башни, выложенной огнеупорным материалом, распыливается подлежащая концентрации серная кислота. Навстречу ей снизу поднимаются горячие продукты горения, получаемые от сжигания кокса, антрацита или нефти. Встречая распыленную кислоту, они увлекают содержащуюся в ней воду; концентрированная серная кислота стекает вниз башни и отводится отсюда особым стоком в холодильник, а из него в сборник.
Аппараты Кесслера и Гайяра в современных условиях считаются наиболее экономными по расходу топлива аппаратами для упаривания камерной серной кислотой до концентрации купоросного масла (66° Б., или 94-95% H2SO4).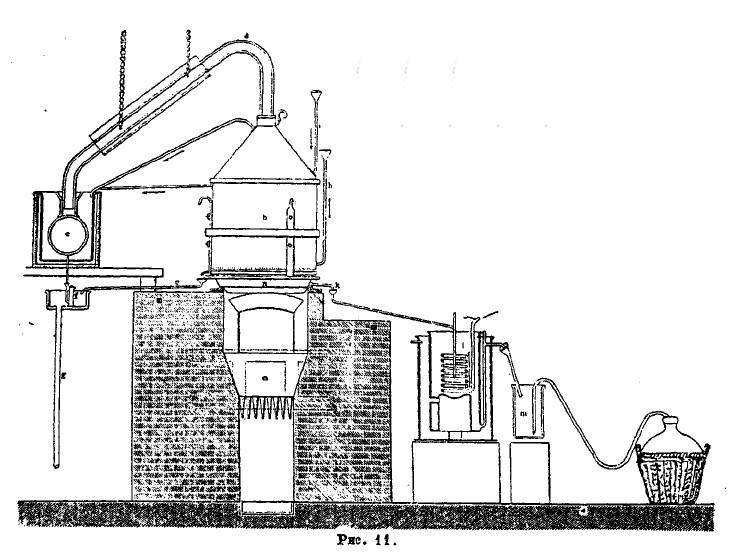
Рис. 11.
2. Контактный способ добывания серной кислоты. Задача полного превращения сернистой кислота (SO2) печных газов в серный ангидрид разрешена была в 1888 г. Баденской анилиново-содовой фабрикой (после обстоятельных исследований Р. Книча). Такое превращение в ангидрид (SO2) в случае разбавленных печных газов при помощи платинированного асбеста удалось настолько хорошо, что стало выгодно в большом масштабе добывать обыкновенную серную кислоту из получаемого контактным процессом ангидрида и таким образом обходиться без свинцовых камер. Процесс образования SО3 — процесс обратимый, сопровождающийся выделением теплоты (экзотермический); SO2 + О ↔ SO2 + 22,6 кал., и подчиняется закону действия масс.
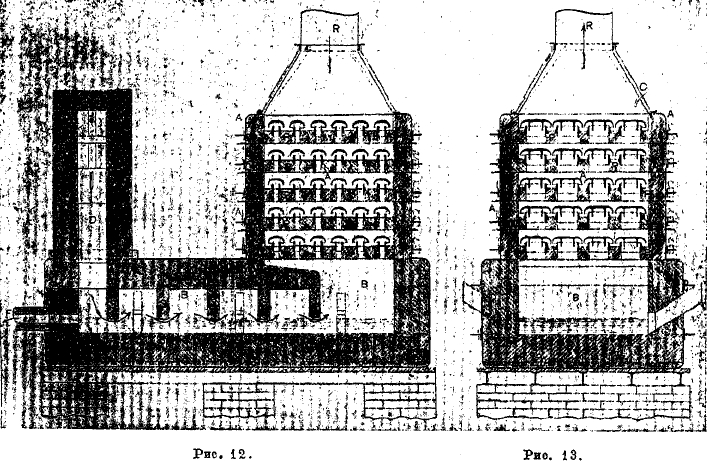
Рис. 12. Рис. 13
С платиной в виде контактной массы, он начинается при 200°, достигает максимума при 400—430° и убывает при более высоких температурах; при 1 000° он вполне обратим, т. е. образующийся SО2 вполне распадается на SO2 и О. При избытке кислорода, например, при молекулярном отношении 2SО2 : 3О2, как это имеет место в печных колчеданных газах с 7% SO2 и 10% О2, почти вполне образуется ангидрид при достаточно продолжительном соприкосновении с платиной при 380—430°. Разбавление газов большим количеством воздуха не имеет существенного значения. Если же возьмем смесь SО2 и О2 в стехиометрическом отношении (2SО2 : О2), то реакция не доходит вполне до конца (ошибка К. Винклера). Пусть а, b и с обозначают количество молекул SO2, О2 и газообразного SО3, содержащегося в 1 куб. м; тогда имеет значение закон: a2b/c2=K, где K — фактор превращения в зависимости от температуры и контактного вещества. Без контактного вещества, SО3 вполне распадается при 1200° на SO2 и О, так что контактное вещество ускоряет не только образование SO2, но и распад его.
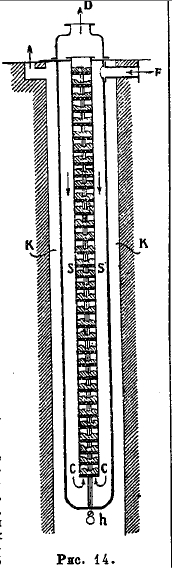
Рис. 14.
Существенно важно для поднятия выходов уменьшение перегрева, получающегося вследствие выделения реакционной теплоты; контактные аппараты даже охлаждают холодными печными газами; эти последние одновременно прогреваются до требуемой реакционной температуры. Рис. 14 представляет трубообразную вертикальную печь Баденской анилиново-содовой фабрики: она состоит из железной трубы R, содержащей насаженные на общий стержень дырчатые полочки с наложенным на них платинированным асбестом, так чтобы между отдельными полочками оставалось промежуточное пространство, а газы проходят чрез трубу, не претерпевая значительного сопротивления. Входящие в Е очищенные холодные печные газы при своем прохождении по кольцевому пространству SS обмывают контактную трубу R, прогреваются насчет реакционной теплоты и при СС попадают в контактную трубу. В последней происходит образование ангидрида (SO3); с ним отработавшие газы оставляют трубу при D. Аппарат таких размеров, что весь процесс протекает самодеятельно; в наружном кожухе KK может циркулировать или холодный воздух, или подогретый горелкой h газ.
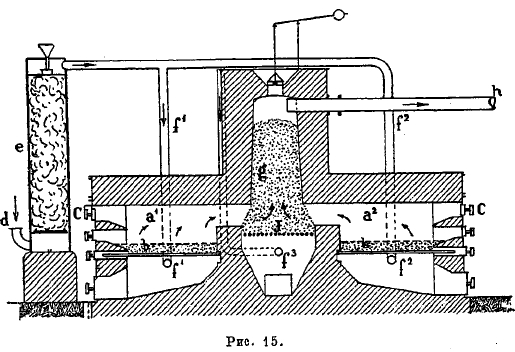
Рис. 15.
Для удачного применения способа существенно важно тщательное очищение печных газов; только тогда контактная масса действует продолжительное время; очищаются газы не только от летучей пыли, но и от всех газообразных и туманных примесей, потому что примешанные мышьяковистые и ртутные соединения*), даже в виде следов, ядовито действуют на контактную массу, и она перестает действовать. Для очищения печных газов на Баденской анилиново-содовой фабрике, прежде всего, в печные газы вдувают водяной пар, вследствие чего содержащаяся в них серная кислота конденсируется в виде более разбавленной кислоты и осаждается в свинцовых трубах, затем газовая струя подвергается тщательному промыванию и фильтрованию, пока химические и оптические пробы будут указывать на полную чистоту их. После этого газы высушиваются, прогреваются и пускаются в контактную трубу. На других заводах пользуются другими контактными способами. Гехстский завод пользуется также платинированным асбестом, зав. Грилло-Шредера применяет контактную массу из растворимых в воде солей вместе с платиной; конечно, такие соли должны оставаться без изменения при контактном процессе.
*) В колчеданах очень часто содержатся небольшие количества мышьяка (а иногда и ртути), которые при обжиге этих руд улетучиваются.
Они сначала переводятся в водный раствор, смешиваются с раствором платиновой соли и выпариваются. Образующуюся корку солей высушивают до удаления воды, дробят на крупные зерна и подвергают реакции выделения металлической платины, после чего они пригодны для контактного процесса. Такими солями предложены МgSO4, ZnSO4. Кроме мелко раздробленной платины, деятельным контактным веществом могут служить окись меди, окись железа, окись хрома, ванадиевая кислота. Союз химических заводов в Мангейме предложил контактный способ получения SO3 при помощи окиси железа, способ, отличающийся на первый взгляд технической простотой, но в практике оказавшийся не вполне удовлетворительным. Контактное действие окиси железа сказалось гораздо сильнее, чем до сего времени предполагали, хотя и не достигает платины; оно объясняется тем, что Fe2O3 попеременно восстановляется в Fe3О4 и снова окисляется в Fe2O3 воздухом, или же образуется сернокислая окись железа, которая и разлагается на Fe2O3 + SО3. Так как полное превращение SO2 в SO3 при помощи Fe2O3 не удается в одну операцию, то главное количество SO3, происшедшее при контакте на окислах железа, удаляется поглощением серной кислоты, остающиеся газы подвергаются вторичному контактному действию при помощи платинированного асбеста. Рис. 15 дает представление об устройстве контактного аппарата по мангеймскому способу. Колчеданные печи а1, а2 герметично заперты, так чтобы воздух по возможности не проникал чрез дверки и щели, и только для загрузки открываются на короткое время в С. Воздух, предназначенный для горения, высушивается в башне е и поступает по f1 и f1 под колосниковую решетку печей. Печные газы, неочищенные и горячие, поступают в контактное пространство g, непосредственно примыкающее к печам; это пространство загружается большим количеством свежих колчеданных огарков. Нижние слои последних задерживают всю пыль и примеси (например, мышьяк в виде мышьяковистого железа), верхние же, при температуре 560—600°, способствуют дальнейшему образованию ангидрида (SО3). Окисложелезный слой, ставший недеятельным, периодически удаляется и заменяется свежими огарками. Газы дальше поступают на охлаждение и поглощение и т. д. Так как газы до поступления в контактный аппарат должны быть тщательно очищены промывкой через воду, слабую серную кислоту, потом высушены, проходя через серную кислоту высшей концентрации, словом, должны совершить длинный путь, преодолевая при промывках значительное сопротивление (от трения), то для приведения их в движение между осушительными аппаратами (башнями) и самим контактным аппаратом ставится мощный эксгаустор (или компрессор), который должен протягивать газы чрез всю систему установок.
К контактным аппаратам всегда примыкают холодильники и конденсаторы. Для охлаждения газов служат вертикальные трубчатые холодильники, в которых горячая газовая смесь охлаждается водою через стенки труб; конденсаторы — оросительные башни или другого типа поглотительные сосуды; в них серный ангидрид вымывается из газовой смеси при помощи концентрированной серной кислоты. Заслуживает внимания, что концентрированная серная кислота с 97— 99% Н2SO4 лучше всего годится для полного улавливания SO3; разбавленная кислота или вода недостаточно поглощают. Вентилятор просасывает газы из колчеданных печей и прогоняет их чрез поглотительные сосуды (башни). Вся система делается, после осушительных башен, из железа и, вместо больших свинцовых камер, действуют аппараты, занимающие небольшое пространство; в них газовая струя (поток) прогоняется эксгаустором (компрессором). Окончательным продуктом при контактном способе получается дымящаяся серная кислота с 20—30% SO3 (масло). Ангидрид можно отогнать от этого масла в чугунных или железных ретортах; остается после отгонки концентрированная серная кислота. Из дымящейся серной кислоты можно добыть обыкновенную кислоту, разбавляя ее серной кислотой или водой; можно приготовить не только 66°-ную серную кислоту, но также 60° и 50°-ную. Все кислоты, получающиеся из ангидрида, отличаются чистотой, особенно в отношении мышьяка, что очень важно в некоторых производствах.
Что касается стоимости устройств аппаратов для получения серной кислоты по контактному способу, то, для больших масштабов, эти устройства обходятся дороже устройств добывания серной кислоты по камерному способу.
В заключение приведем описание одного из современных контактных заводов, работающих в СССР.
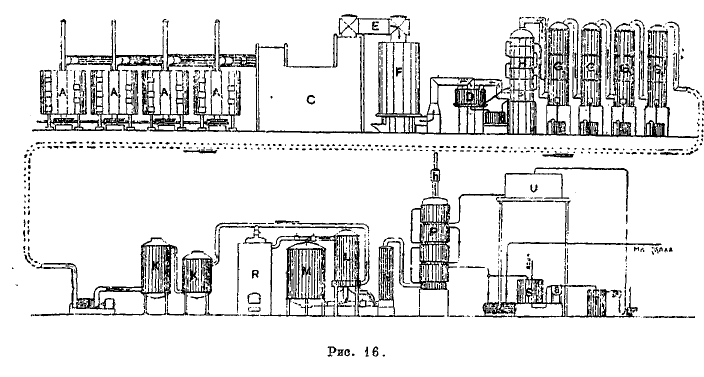
Рис. 16.
Рис. 16 представляет схему расположения аппаратуры для производства серной кислоты по контактному способу Тентелевского завода (в Ленинграде). Для сжигания серного колчедана (в виде мелочи) служат механические печи Герресгофа; их 4 (A1, А2, А3, А4), каждая производительностью 3 тонны колчедана в сутки. Из печей печные газы по сборной трубе В поступают в пыльную камеру С, в которой газ очищается от пыли и отчасти мышьяка и затем по трубе Е поступает в холодильник F; здесь газ, пройдя холодильник, охлаждается с 300—400°С до 90—120°серы и поступает в промыватель газа, называемый «форвашером», для освобождения газов от сопровождающих их, вредных для катализатора, примесей (ядов). Из форвашера газы направляются в промывную башню Н, где газы энергично промываются водой и совершенно освобождаются от вредных для катализатора примесей. Из промывной башни газ поступает в четыре последовательно соединенных сушильных башни G1, G2, G3, G4. Все башни смонтированы из листового свинца и насажены коксом. Первая башня служит как бы фильтром для улавливания механически увлекаемых газом частиц воды; в остальных трех кокс орошается серной кислотой, стекающей по коксу сверху навстречу поднимающемуся газу. Крепость серной кислоты различная: во второй башне G2 она 58°Б., в третьей 60°Б. и в последней (G4) около 66°Б. Такой крепости серная кислота осушает газ. Из последней башни газ поступает в компрессор J, который необходим вследствие наличия значительных сопротивлений в отдельных аппаратах. Разрежение пред входом газа в компрессор достигает 10—13 см ртутного столба, а давление газа за компрессором составляет 15—20 см того же столба. Из компрессора газы поступают в последовательно включенные маслоотделители К-К (это фильтры, насаженные: первый коксом, второй волокнистым асбестом). Назначение маслоотделителей — выделить из газа то смазочное масло, которое попадает в газ из компрессора. Пройдя маслоотделители, газ поступает в т. н. «температурный регулятор» L; здесь холодный очищенный газ подогревается теплотой газа, выходящего из контактного аппарата. «Температурный регулятор» сконструирован по принципу рекуператора: горячий газ, выходящий из контактного аппарата, поступает в ряд трубок, которые омываются холодным газом, поступившим из маслоотделителей.
Из температурного регулятора L подогретый газ направляется в контактный аппарат М, состоящий из ряда вертикально поставленных трубок, особым способом заполненных платинированным асбестом. В контактном аппарате происходит окисление SО2, содержащегося в газе, в SO3. Газ входит в контактный аппарат с температурой 220—240°С и выходит из него с температурой 400—450°С и температурный регулятор L. Повышение температуры реакции обусловливается экзотермичностью реакции окисления SО2 в SO3. Горячие газы из контактного аппарата обратно поступают в терморегулятор, нагревают там холодный газ, идущий в контактный аппарат, охлаждаясь до температуры 300—350°С, и поступают в ангидридный холодильник N, состоящий из ряда вертикальных стальных труб охлаждаемых атмосферным воздухом. Пройдя этот холодильник, газы направляются в абсорбер (поглотитель) Р для поглощения SO3 из газа, с целью получения олеума (дымящейся серной кислоты). Отработанные газы, не содержащие SO3, по трубе h выходят в атмосферу. Из абсорбера Р часть олеума поступает в монтжю G и перекачивается на склад, другая часть поступает в «смеситель» S, где происходит смешение олеума с водой с образованием 96—98% серной кислоты, которая поступает в холодильник а и Т и эмульсером n подается в бак U, из которого перетекает в абсорбер Р.
Здесь нами описана схема расположения аппаратов Тентелевского завода. Работают также и другие системы, например, очень распространенная в СССР система расположения аппаратов Грилло—Шредера. Главная особенность та, что в этой системе контактный аппарат наполнен не платинированным асбестом, а зернами безводного сернокислого магния с осажденной на них платиной. Для подогревания холодного газа, поступающего на контакт, должен работать все время подогреватель газа пред контактным аппаратом, где газ подогревается, до 330—360°С. В других системах платина осаждается на керамических небольшого размера цилиндрах, на зернах кварца, на алюминиевой дроби (шариках). Главное, к чему стремятся все эти видоизменения осаждения платины в виде тонкого слоя, это — создание наибольшего поверхностного слоя платины наибольшей толщины и наибольшего ее активного действия; тем самым уменьшается расход платины и, следовательно, понижается основной капитал, затрачиваемый на оборудование завода. Подробности см. Лукьянов П. М., «Курс химической технологии минеральных веществ», ч. 1.
Необходимость огромного количества серной кислоты для получения взрывчатых веществ выдвинула во время войны на первый план вопрос о добывании кислоты из имеющихся сернокислых солей, в первую очередь из гипса, образующего мощные залежи во многих местах, в тех странах, где своего серного колчедана или мало, или совсем нет (Германия). Задача была решена следующим способом. Смесь гипса с углем и глиноземом в присутствии небольшого количества окиси железа подвергают накаливанию в длинных (до 60 м) вращающихся печах, сходных с цементными. Происходит процесс восстановления с выделением сернистого ангидрида, который уже обычными способами превращается в серную кислоту. Остающийся твердый продукт представляет превосходный цемент, нашедший себе широкое распространение.
3. Производство серной кислоты в важнейших странах видно на следующей таблице:
|
Страны |
Перед войной |
1918 г. |
1923 г. |
|
В тыс. тонн многидрата |
|||
|
Великобритания |
1500 |
- |
876 |
|
Германия |
1700 |
1009 |
714 |
|
Франция |
1200 |
2550 |
- |
|
Соединенные Штаты |
36001) |
75001) |
61801) |
1) Для С. Ш. взят не моногидрат, а 50% серной кислоты.
Серной кислоты, перечисленной на 100% кислоту, производилось у нас в годы:
1911 г. – 203 тыс. т;
1916 – 261;
1917 – 340;
1925/26 – 93.
Увеличение производства серной кислоты в годы 1917—1918 было вызвано военным временем, когда потребление ее значительно возросло с производством взрывчатых веществ, нужных для военных целей.
Что касается до потребления серной кислоты в мирное время, то это лучше всего объясняют следующие данные: в 1911 г. Германия добыла 1 700 000 тонн серной кислоты, т. е. в 7—9 раз больше, чем Россия. Из этого количества она тратила:
На суперфосфатное дело 42% всей выработки
« серноаммиачное « .... 20% « «
« глиноземные соли 1,5% « «
« сульфатное дело 20% « «
83,5%
Остальные же 16,5% уходило на взрывчатые вещества, производство красителей и пр. Эти 16,5% всей выработки серной кислоты составляют 280 500 тонн, т. е. Германия в 1911 г. на взрывчатые вещества и производство красителей тратила столько, сколько наша промышленность смогла дать этой кислоты (наибольшую выработку) в военное время при своем наивысшем напряжении; в данное же время наша химическая промышленность дает серной кислоты вдвое меньше, чем она давала в 1911 г. О производстве и потреблении серной кислоты в Соединенных Штатах см. химическая Промышленность, XLV, ч. 2, 259.
4. Применение серной кислоты. В современной культурной жизни серная кислота представляет один из важнейших материалов. Камерная серная кислоты в 50—53°Б. употребляется для приготовления разбавленной серной кислоты, которая находит применение при белении тканей для удаления следов хлорной извести. Кислота в 60—62°Б. (или гловерова кислота) употребляется для приготовления сульфата или сернонатриевой соли, сернокалиевой соли, одновременно для добывания соляной кислоты (побочно хлорной извести, бертоллетовой соли, соды, стекла, мыла); для добывания многих кислот: кроме соляной кислота, — азотной, сернистой, фосфорной, борной, хромовой, угольной, щавелевой, виннокаменной, уксусной, лимонной, стеариновой, пальмитиновой, олеиновой; для фабрикации суперфосфатов, кислого фосфорнокислого кальция; для получения фосфора, иода, брома, хлора, аммониевого сульфата, баритового сульфата (краска блан-фикс); при фабрикации стеарина и стеариновых свеч; для добывания глиноземного, железного и медного купоросов, для приготовления хромовых квасцов, при получении хромпика; в металлургии: для получения солей магния, алюминия, меди, ртути, кобальта, никеля и т. д.; для протравления и очищения железа при покрытии его цинком или оловом; для гальванических элементов, — таким образом: в телеграфии, телефонии, для гальванического серебрения и золочения; для получения водорода и перекиси водорода; для добывания обыкновенного эфира и искусственных эфиров; при приготовлении гарансина и других краповых препаратов (искусственного ализарина); для добывания и очищения многих органических красок, растительных и минеральных масел (например, рапсового, солярового, керосина, парафина); для приготовления пергаментной бумаги; для получения крахмальной патоки и крахмального сахара, для осахаривания сусла (заторов); для усреднения щелочной реакции в жидкостях, предназначенных для брожения; для разрушения растительных волокон в смешанных тканях. Обыкновенная (английская) концентрированная серная кислота в 65—66°Б. употребляется: для добывания жирных кислот при перегонке их; для очищения рапсового масла; для фабрикации пироксилина (коллодия), пикриновой кислоты, нитробензола, нитронафталина, тротила (тринитротолуола) и других легко нитруемых тел; для очищения бензола, керосина, парафинового и минеральных масел; для добывания кислорода из перекиси марганца; для высушивания воздуха, хлорного газа и других технических целей. Концентрированная серная кислота в 66°Б: для рафинирования золота и серебра, для добывания взрывчатых веществ, нитроглицерина; для сульфурирования органических тел (в каменноугольно-дегтярной красочной промышленности). Дымящаяся серная кислота употребляется для растворения индиго, для добывания ализарина, резорцина и многих органических сульфокислот; для очищения озокерита при приготовлении ваксы. Серный ангидрид в большей или меньшей степени может заменять дымящуюся серную кислоту. Чистая серная кислота различных концентраций находит применение в химических исследованиях; кроме того, в фармации и медицине (как противоядие против свинцовых отравлений; как антисептик, например, при кровяном распаде). Из этого длинного перечня применения серной кислоты явствует, какое громадное значение имеет она в культурной жизни всякой страны: те страны, в которых добывается серная кислота в громадных количествах, —например, Германия, Англия, Франция — отличаются высокоразвитой химической промышленностью.
Литература: Н. Любавин, «Техническая химия», І т.; Федотьев, «Производство серной кислоты». В этих двух книгах обстоятельно изложены старые способы добывания серной кислоты в камерах. Лукьянов, П. М., «Курс технологии минеральных веществ», ч. 1-я, 1924; он же, «Производство серной кислоты методом контактного окисления», 1922; Ullmann, «Enzyklopädie der technischen Chemie», т. Х, 1922; G. Lungе, «Handbuch der Schwefelsäurefabrikation», 1916 (в 2 т.). Последняя книга считается классической по производству серной кислоты. Что касается до новостей последнего времени, то их надо искать в текущей журнальной иностранной и русской литературе, например: «Zeitschr. für angew. Chemie»; «Журнал русской химической промышленности», изд. в Москве; Орлов, Е. И., «Германская крупно-химическая промышленность в годы до войны», 1917. Эта брошюра дает статистику химической промышленности в довоенное время.
Е. Орлов.
| Номер тома | 41 (часть 6) |
| Номер (-а) страницы | 566 |
