Сталь
Сталь
I. ЧТО ТАКОЕ сталь. Наиболее общим ответом на вопрос — «что такое сталь» может служить следующее определение: сталь есть обладающий свойством ковкости продукт железоделательного производства (см.). Положить в основу определения стали какой-либо более конкретный признак представляется невозможным ввиду чрезвычайного разнообразия свойств стали: сталь может быть мягкой и очень твердой, пластичной и упругой, прочной и хрупкой, магнитной и немагнитной, легко проводящей электрический ток и обладающей высоким электросопротивлением, легко окисляющейся и нержавеющей, обладающей весьма различающимися коэффициентами линейного теплового расширения и т. д.

Фиг. 1. Строение твердой стали, содержащей около 1% стали, видимое в микроскоп при увеличении в 450 раз: пластинчатый карбид в железе (Беляев и Гудцов).

Фиг. 2. Строение той же стали, что и на фиг. 1, при том же увеличении, после тепловой обработки: глобулярный карбид железа в железе (Беляев и Гудцов).
Причины разнообразия свойств стали весьма многочисленны — их можно объединить в четыре основные группы факторов: 1 — факторы химического характера; 2 — факторы кристаллографического характера; 3 — факторы физического характера и 4 — факторы механического характера (ср. металлография).
1. Химический состав стали. Основной элемент, входящий в состав стали — железо; содержание его обычно не бывает ниже 90%; лишь в случае изготовления стальных сплавов особого назначения содержание железа понижается и доходит иногда до 70% и даже 50%. Остальные элементы, входящие в состав стали, могут быть либо обычными спутниками железа, неизбежно остающимися в стали при различных способах ее изготовления,— таковы: углерод, кремний, марганец, сера, фосфор и газы (азот и кислород, входящие в состав твердых определенных соединений, водород, образующий твердый раствор с железом); либо специально вводимыми при выплавке с целью изменения качеств сталь примесями, — таковы: кремний и марганец в избыточном против обычного количестве, никель, медь, алюминий, хром, ванадий, молибден, вольфрам, кобальт, титан, цирконий, уран, бор, церий.
Принимая во внимание возможное количественное разнообразие содержания отдельных примесей, а также учитывая то обстоятельство, что при изготовлении стали не всегда ограничиваются введением какой-либо отдельной примеси, но сплошь и рядом вводят два, три и даже четыре различных элемента одновременно, можно математически вычислить возможное число различных комбинаций состава стали — число это бесконечно велико.
Каждый введенный в сталь добавочный элемент в очень редких случаях существует самостоятельно, обычно он образует твердые растворы с железом или с другой примесью, либо растворяясь непосредственно, либо образуя новые тела — определенные соединения, в состав которых входят помимо данного элемента также железо или какие-либо из других примесей стали. Так, углерод, основная и обязательная примесь стали, обладающий способностью частично растворяться в железе при известных температурных условиях, образует определенное соединение с железом, так называемый карбид железа, Fe2С. Помимо того, углерод может также существовать в стали самостоятельно, в форме весьма близкой или аналогичной состоянию графита. Кремний образует твердые растворы, как с железом, так и с карбидом железа (Gentermann, Upton, Байков). Марганец образует определенные соединения с серой — сернистый марганец MnS, и с углеродом — Мn2С — карбид марганца, кроме того марганец дает твердый раствор непосредственно с железом. Сера образует определенные соединения с железом и марганцем (нерастворимые в железе) и с цирконием. Хром образует соединения с углеводом двух типов: Cr3C2 и Сr4С; кроме того, легко образует с железом твердые растворы. Приведенные примеры достаточно наглядно иллюстрируют то усложнение в составе стали, которое вносится существованием различных определенных соединений элементов, входящих в состав стали.
Последнее обстоятельство, — возникновение определенных соединений элементов с железом и друг с другом, — служит также механизмом для усиления влияния каждой отдельной примеси, и механизмом иногда чрезвычайно сильнодействующим, в чем можно убедиться на примере основной и главнейшей примеси стали, углерода. При образовании карбида железа, Fe3С, каждая одна весовая часть углерода дает пятнадцать весовых частей карбида (точнее — 14,96). Следовательно, содержанию в стали углерода в количестве 0,1% в действительности соответствует содержание 1,5% карбида железа, а 1% углерода соответствует 15% карбида. Далее, карбид железа, называемый часто в металлографии «цементитом» в редких случаях присутствует в стали изолированно от основной массы железа; обычно же карбид распределяется в виде очень мелких, видимых лишь в микроскоп, образований, имеющих форму либо мелких и тонких пластинок (фиг. 1), либо глобулей округленной формы (фиг. 2) в некотором объеме железа. Эти объемы железа, насыщенные мелкими карбидными образованиями, по своему виду резко отличаются при микроскопическом изучении структуры от основной железной массы, как показывает микрофотограмма (фиг. 3), изображающая строение стали, содержащей 0,4% С, при увеличении в 100 раз. По своим механическим свойствам и, главным образом, по твердости такая механическая смесь железа и карбида железа значительно отличается от чистого железа. Кроме того, соотношение между железом и карбидом железа в смеси более или менее постоянно и может быть приблизительно выражено в круглых числах отношением 7:1. Оба эти соображения заставляют считать механическую тесную смесь карбида железа и железа за особую самостоятельную составляющую при изучении строения стали, большее или меньшее присутствие которой значительно изменяет свойства стали. Подобного рода смеси известны в физической химии под названием эвтектических (если они образуются при застывании сплава) или эвтектоидных (если они образуются в затвердевшем уже сплаве) смесей. Эвтектоидная смесь железа и карбида железа получила особое название «перлит», в отличие от основной массы железа, называется в металлографии «ферритом».

Фиг. 3. Строение стали средней твердости, видимое в микроскоп при увеличении в 100 раз. Светлые места - железо (феррит), темные места — смесь железа и карбида железа (перлит) (Беляев и Гудцов).
Принимая за близкое к действительности указанное выше соотношение составных частей перлита: 7 частей железа на 1 часть карбида железа, можно уяснить себе механизм дальнейшего усиления влияния углерода на свойства стали: для этого вычисленный ранее коэффициент 15 приходится увеличить еще в 8 раз, что дает в результате новый коэффициент 120. Таким образом, весьма малое содержание в стали углерода, например в количестве 0,1% дает уже вполне ощутимое содержание карбида 1,5%, что в свою очередь равносильно присутствию перлита в количестве около 12%, т. е. около 1/8 всего объема стали. Профессор А. Sauveur составил следующую таблицу теоретического структурного состава стали, не содержащей других примесей, при различном содержаний углерода (см. табл. 1).
Таблица эта показывает, что уже при содержании в стали 0 8% углерода почти весь ее объем оказывается состоящим из одного только перлита (96%). Теоретически можно подсчитать, что при 0,834% С содержание перлита в стали достигнет 100%, т. е. весь объем стали окажется состоящим из эвтектоидной смеси железа и карбида железа, по своим физическим и механическим свойствам значительно отличающейся от железа. Дальнейшее возрастание содержания карбида создает избыток карбида по сравнению с тем его количеством, которое требуется для построения перлита. Избыточный карбид, не входящий в эвтектоидную смесь, существует в стали как самостоятельная составляющая структуры, что, неизбежно, приводит к новому изменению основных свойств стали, так как карбид железа является телом, совершенно отличным по свойствам от железа и перлита: он очень тверд, хрупок и обладает малой способностью к деформированию. Последний столбец таблицы 1-й показывает содержание в стали избыточного, свободного карбида при содержании углерода более 0,834%.
Таблица 1.
Химический и структурный состав идеальной (без примесей) углеродистой стали (А. Sauveur).
|
Химический состав в % |
Структурный состав в % |
|||||
|
Конечный |
Конечный |
Действительный (приблизительный) |
||||
|
C |
Fe |
Общее содержание карбида |
Общее содержание феррита |
Перлит |
Свободный графит |
Свободный карбид |
|
0,1 |
99,9 |
1,5 |
98,5 |
12,0 |
88,0 |
- |
|
0,2 |
99,8 |
3,0 |
97,0 |
24,0 |
76,0 |
- |
|
0,3 |
99,7 |
4,5 |
95,5 |
36,0 |
64,0 |
- |
|
0,4 |
99,6 |
6,0 |
94,0 |
48,0 |
52,0 |
- |
|
0,5 |
99,5 |
7,5 |
92,5 |
60,0 |
40,0 |
- |
|
0,6 |
99,4 |
9,0 |
91,0 |
72,0 |
28,0 |
- |
|
0,7 |
99,3 |
10,5 |
89,5 |
84,0 |
16,0 |
- |
|
0,8 |
99,2 |
12,0 |
88,0 |
96,0 |
4,0 |
- |
|
0,9 |
99,1 |
13,5 |
86,5 |
98,7 |
- |
1,3 |
|
1,0 |
99,0 |
15,0 |
85,0 |
97,0 |
- |
3,0 |
|
1,1 |
98,9 |
16,5 |
83,5 |
95,3 |
- |
4,7 |
|
1,2 |
98,8 |
18,0 |
82,0 |
93,6 |
- |
6,4 |
|
1,3 |
98,7 |
19,5 |
80,5 |
91,9 |
- |
8,1 |
|
1,4 |
98,6 |
21,0 |
79,0 |
90,2 |
- |
9,8 |
|
1,5 |
98,5 |
22,5 |
77,5 |
88,5 |
- |
11,5 |
|
1,6 |
98,4 |
24,0 |
76,0 |
86,8 |
- |
13,2 |
|
1,7 |
98,3 |
25,5 |
74,5 |
85,1 |
- |
14,9 |
|
1,8 |
98,2 |
27,0 |
73,0 |
83,4 |
- |
16,6 |
|
1,9 |
98,1 |
28,5 |
71,5 |
81,7 |
- |
18,3 |
|
2,0 |
98,0 |
30,0 |
70,0 |
80,0 |
- |
20,0 |
Таблица поправок
|
При увеличении содержания углерода в %% на |
Для стали, содержащей 0,8% и менее углерода, к содержанию перлита в % должно быть прибавлено и от содержания феррита в % отнято |
Для стали, содержащей 0,9% и более углерода, и содержащей карбида в % должно быть прибавлено и от содержания перлита в % отнято |
|
0,01 |
1,2 |
0,17 |
|
0,02 |
2,4 |
0,34 |
|
0,03 |
3,6 |
0,51 |
|
0,04 |
4,8 |
0,68 |
|
0,05 |
6,0 |
0,85 |
|
0,06 |
7,2 |
1,02 |
|
0,07 |
8,4 |
1,19 |
|
0,08 |
9,6 |
1,36 |
|
0,09 |
10,8 |
1,53 |
Влияние многих других примесей стали также усиливается при помощи образования определенных соединений и эвтектоидных смесей, что и заставляет при определении химического состава стали обращать серьезное внимание на столь малые вариации в содержании отдельных примесей, как 0,1%.
Неоднократно делались попытки выделить как основной признак стали, отличающий ее, с одной стороны, от железа, с другой стороны, от чугуна, — содержание в ней углерода. Как отдельными исследователями, так и коллективно на съездах, конференциях, делались попытки установления того предельного содержания углерода, которое должно было считаться за минимальное для стали и максимальное для железа; но в жизни все эти попытки оказывались бесполезными, так как заводская металлургическая практика не укладывалась в отводимые рамки, в особенности после того, как в большом количестве на заводах стала изготовляться сталь с различного рода специальными примесями. Считая, поэтому, установление границы по содержанию углерода между железом и сталью бесполезным и бесцельным, мы должны признать за правило, следуя предложению немецкого исследователя стали G. Mars'а, то, что давно уже установлено металлургической практикой, а именно, называть сталью все те продукты железоделательного производства, которые получаются в жидком расплавленном виде в различного рода печах и устройствах (бессемеровские и томасовские конвертеры, мартеновские, тигельные, электрические печи), а железом — все продукты, получаемые не в расплавленном состоянии.

Фиг. 4. Кристалл Чернова. 1/6 натуральной величины.
Со значительно большей определенностью может быть указана граница по содержанию углерода между сталью и чугуном: сталь содержит углерода не более 2%; чугун — не менее 2,5%. Промежуточную между сталью и чугуном область занимают такие продукты, как ковкий чугун и цементная сталь (последняя в настоящее время почти не приготовляется).
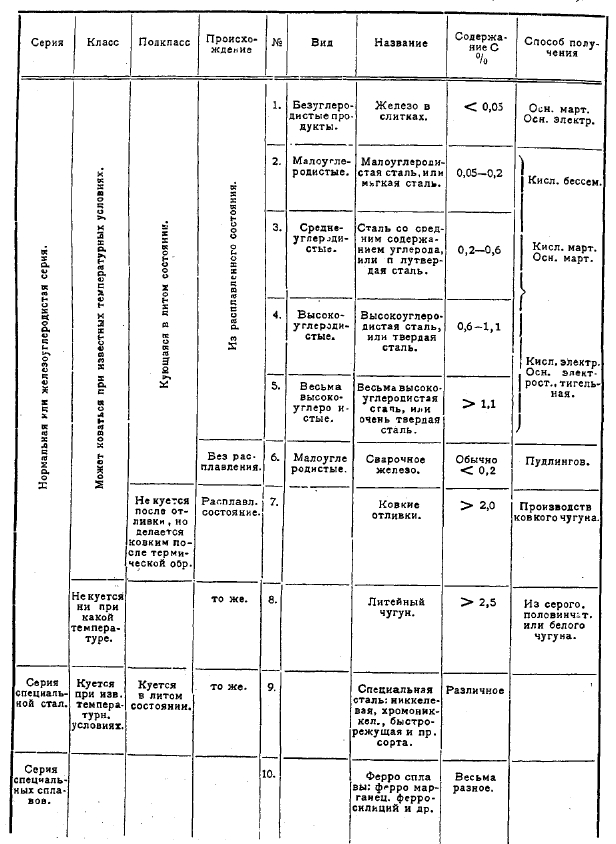
Место, занимаемое сталью среди всех продуктов железоделательного производства, можно видеть в табл. 2-й, заимствованной у американского металлурга F. Т. Sisco (Transact. Am. S. St. Treat. VIII, 1925, стр. 194).
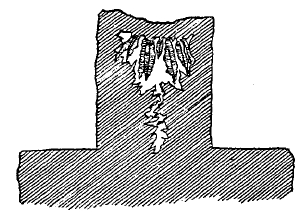
Фиг. 5. Кристаллы стали в прибыльной части большого слитка (по Д. К. Чернову).
2. Кристаллическое строение стали. Как и все прочие твердые металлические сплавы, сталь — тело кристаллическое. Внешнее кристаллическое строение стали проявляется во всех тех случаях, когда на поверхности затвердевающего металла не встречается каких-либо препятствий к образованию правильных кристаллических форм. Такие кристаллы и друзы кристаллов стали часто находятся во внутренних пустотах больших слитков стали; большой известностью пользуется кристалл Чернова (фиг. 4), найденный Д. К. Черновым в раковине (внутренняя пустота) большого слитка твердой мартеновской стали Обуховского завода, весившего около 100 тонн. Верхняя часть этого слитка, так называемая прибыль, разрез которой, схематически зарисованный самим Д. К. Черновым, изображен на фиг. 5, имела размеры в диаметре 990 мм и по высоте 1500 мм. Вес кристалла Чернова 3 45 кг, длина — 390 мм.

Фиг. 6. Большой кристалл стали длиной в 480 мм (по Primrose).
На фиг. 6. изображен другой интересный кристалл стали, отысканный I. S. G. Primrose (Англия) в 50-тонном слитке мягкой мартеновской стали; кристалл этот весит 1 35 кг и в длину достигает 480 мм. Фиг. 7 изображает весьма редкие образцы шаровидных затвердевших брызг стали, покрытых с поверхности целыми друзами мелких кристалликов. Образцы эти были найдены профессором В. Е. Грум-Гржимайло на одном из южнорусских металлургических заводов.
Поперечный разрез одного из кристаллов средней величины, найденный Н. И. Беляевым на Путиловском заводе в стальном слитке, представлен на фиг. 8. Кроме того, на фиг. 9 показано кристаллическое строение поверхности стальной лепешки очень медленно застуженной (Н. И. Беляев).

Фиг. 7. Мелкие кристаллы стали. Ib. 1,75.

Фиг. 8. Поперечный разрез кристалла стали (по Н. И. Беляеву).
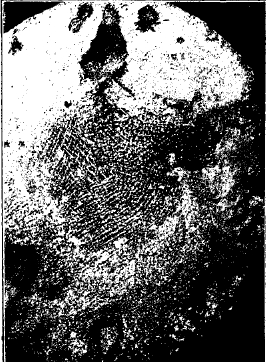
Фиг. 9. Наружная поверхность стальной лепешки, очень медленно затвердевшей под слоем шлака (по Н. И. Беляеву).
Таблица 2
Номенклатура продуктов железоделательного производства (F. T. Sisco).
Обычно, в заводских условиях получения слитков стали, поверхность слитков не имеет правильной кристаллической формы; в то же время весь объем металла строится согласно законам кристаллографии, образуя большее или меньшее количество отдельных замкнутых объемов с одинаковым расположением кристаллических осей элементарных кристалликов. Поверхности соприкосновения отдельных таких пространственных областей или зерен легко обнаруживаются при травлении кислотой полированной поверхности разреза стального тела — во-первых, по различному направлению кристаллических осей по ту и другую сторону пограничной поверхности; во-вторых, по тому тонкому пограничному слою, который неизбежно должен образоваться для заполнения промежутков между соседними кристаллами, принадлежащими к различным зернам. В разрезе эти тонкие пограничные прослойки между зернами дают рисунок некоторой сетки большей или меньшей величины. Количество и величина зерен, заполняющих данный объем металла, зависят от количества первоначальных зародившихся элементарных кристалликов, называемых в этом случае «центрами кристаллизации», вокруг которых происходит нарастание новых зарождающихся кристалликов с сохранением направления осей кристаллизации первоначальных кристалликов, вплоть до встречи с кристалликами иной ориентации, нарастающими вокруг ближайшего соседнего центра кристаллизации. Механизм нарастания кристалликов и образования зерен хорошо иллюстрирует схема фиг. 10, разработанная профессором W. Rosenhain’ом.
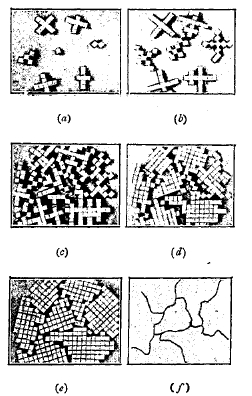
Фиг. 10. Схематическое изображение процесса роста кристаллов и образования кристаллических зерен внутри металла (по W. Roscnhain).
Действительное построение стали из зерен показано на фиг. 11, полученной при фотографировании отполированной и травленой поверхности разреза образца медленно затвердевшей стали из коллекции, приготовленной Н. И. Беляевым, при увеличении в 2,5 раза. Фотограмма фиг. 11 показывает также, что в одном и том же объеме сталь одного и того же химического состава могут быть получены зерна разной величины: более мелкие (направо) и во много раз более крупные (налево). Несомненно, в правой части, затвердевшей более быстро, образовалось первоначально значительно большее число центров кристаллизации, чем в левой части, затвердевавшей и охлаждавшейся очень медленно.
Следовательно, величина зерен, образующихся при затвердевании и кристаллизации стали, находится в непосредственной зависимости от условий затвердевания и охлаждения и может быть получена большей или меньшей для одной и той же стали. Но, с другой стороны, построение стали из зерен крупных или мелких не может не отразиться на механических свойствах всего объема стали, так как общая величина каждого отдельного свойства суммируется из 1) свойств отдельных нормально построенных кристалликов, расположенных внутри каждого отдельного зерна, и 2) свойств ненормально построенных кристалликов пограничного слоя между отдельными зернами (существует и имеет своих сторонников гипотеза, предполагающая аморфное некристаллическое скопление частиц металла в пограничном между зернами слое). Изменение величины зерен изменяет соотношение между количеством нормально построенных и ненормально построенных кристалликов (или аморфного металла) и тем самым оказывает существенное влияние на величину каждого в отдельности механического свойства всего объема стали в целом.

Фиг. 11. Зернистое строение медленно затвердевшей стали. Увеличение 1,6 раза.
Весьма показательны и интересны в этом отношении результаты опытов Н. Т. Angus и Р. F. Sumмеrs, установивших прямолинейную (фиг. 12) зависимость между твердостью металла (медь) и величиной поверхности всех зерен, образующих испытываемый объем металла, в то время как зависимость того же свойства твердости от величины самих зерен металла выражается некоторой более сложной кривой линией параболического типа.
Общеизвестен факт большой хрупкости стали, обладающей крупнозернистым кристаллическим строением обратно, сталь считается тем лучше обработанной, чем мельче величина ее кристаллических зерен.
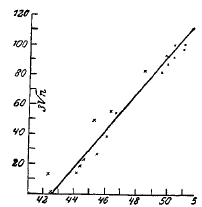
Фиг. 12. Зависимость между величиной поверхности зерен металла (кв. мм/куб. мм) и твердостью металла (по Angus and Summers).
3. Физическое строение стали. Современное физическое учение о природе и строении кристаллических тел заставляет нас представлять себе каждый объем стали построенным из отдельных атомов, расположенных в форме кристаллической решетки. Вид, форма и основные размеры решетки — различны для различных тел. Расположенные в решётку атомы связываются между собой силами двоякого рода: 1) силами, стремящимися удержать и сохранить определенную форму решетки — силы упругости, и 2) силами, стремящимися противодействовать увеличению расстояний между отдельными атомами и разъединению их — силы прочности. Совокупность тех и других сил является главнейшим фактором, предопределяющим основные механические свойства металла: его упругость и прочность.
Но так как сталь — тело сложное, составленное из отдельных элементов, твердых растворов и определенных соединений, то при установлении величины междуатомных сил чрезвычайно важным обстоятельством является существование сил сцепления различной величины, свойственной каждому отдельному телу, участвующему в построении определенного объема стали. Присутствие атомных построений с более низкими силами сцепления, относительное количество такой слабой в механическом смысле структурной составляющей не может не отразиться на общей суммарной величине того или иного свойства куска стали. Но не только одно присутствие тела с иными силами сцепления атомов представляется имеющим такое определяющее значение. Не менее важно также развитие сил сцепления в областях пограничных, где конечные предельные атомы одного кристаллического построения соприкасаются близко с такими же предельными атомами другой по форме кристаллической решетки.

Фиг. 13. Твердые неметаллические включения в стали (Увеличение 500).
В пограничной области могут действовать силы сцепления разнородных атомов: а) либо превышающие силы сцепления однородных атомов каждого из соприкасающихся тел, б) либо промежуточные между силами сцепления соприкасающихся тел, в) либо более низкие, чем силы сцепления соприкасающихся тел. В первом случае наблюдается явление, аналогичное явлению капиллярности, смачивания, и происходит несомненное усиление всего сложного тела, построенного из разнородных кристаллических образований (пример — карбид железа и железо в стали); в последнем случае, наоборот, происходит не усиление, а более или менее значительное ослабление сложного тела, зависящее от абсолютной величины сил сцепления в пограничных областях (пример, сернистые металлы, окислы металлов, с одной стороны, и железо, с другой, в стали). Подобного рода пониженные силы сцепления в пограничных областях могут быть отмечаемы всегда, когда в сталь попадаются так называемые твердые неметаллические включения: шлаки, сернистое железо, сернистый марганец, закись железа, закись марганца, окись алюминия. Такое включение можно видеть на фиг. 13, изображающей при увеличении в 500 раз строение стали, применяемой для изготовления лопат: на общем однообразном фоне весьма резко выделяются темные полоски вытянутых при прокатке неметаллических включений.
Еще более нежелательными особенностями строения стали являются всевозможные случаи нарушения непрерывности строения стали. Сюда относятся случаи: мелкие, часто даже микроскопические пустоты, образующиеся в сталь как пузырьки, наполненные газом, или как раковинки при застывании жидкой стали; мелкие внутренние трещинки, разрывы и надрывы, образующиеся при слишком быстром нагревании стали, при волочении стальной проволоки, при долговременной работе стального изделия. Присутствие в стали хотя бы и чрезвычайно малых по размеру пространств, не заполненных кристаллическими решетками, неизбежно создает напряженное состояние в слое атомов, окружающем незаполненное пространство, в сильной степени понижающее прочность всего объема, вследствие легкости разъединения напряженных атомов этого слоя и образования трещин больших размеров.
Немаловажное влияние на свойства стали оказывает также и характер расположения в стали атомов углерода, главнейшей и неизбежной примеси железа. Углерод, растворенный в железе, не может вызывать разнообразия сил сцепления и потому в сильной степени содействует повышению качеств стали. Углерод, соединенный с атомами железа, образует тело, обладающее весьма большими силами сцепления с прилегающими атомами железа, и в этой форме содействует возрастанию прочности стали. Углерод, существующий самостоятельно (графит в чугуне, аморфный углерод в стали), наоборот, по характеру сил сцепления с железом может быть отожествлен с группой неметаллических включений и, следовательно, в такой форме способен сильно понижать прочность металла.
Таким образом, существование: а) разнообразных сил сцепления однородных атомов, б) разнообразных сил сцепления разнородных атомов, в) возможность случаев нарушения непрерывности строения металла — все эти обстоятельства, характеризующие физическое строение стали, являются в то же время причинами чрезвычайного разнообразия свойств стали даже при одном и том же химическом ее составе.
4. Механическая неоднородность стали. Помимо тех сил сцепления, которые действуют между атомами тел, составляющих какой-либо объем стали, и являются основным фундаментом физического строения стали, в различных изделиях, изготовляемых из стали путем заводской обработки, связанной с изменением формы металла в горячем состоянии (прокатка, ковка), с нагреванием металла до различных температур и охлаждением от этих температур с различной быстротой (после ковки, при закалке), внутри металла могут возникать новые силы, направленные обычно противоположно силам сцепления; эти силы могут быть приблизительно охарактеризованы теми новыми добавочными напряжениями (отношение величины силы к площади сечения, в котором действует сила), которые возникают в некоторых частях объема металла обрабатываемого изделия и носят название «скрытых» или «внутренних» напряжений.
По отношению к силам сцепления эти скрытые напряжения могут быть; а) более низкими по величине — в этом случае получается лишь ослабление прочности изделия на величину, соответствующую величине скрытых напряжений; б) превышающими силы упругости металла, но не постигающими все же величины сил прочности {прочного сцепления атомов) — в этом случае скрытые напряжения вызывают явление как бы самопроизвольного изменения формы металла, называемого в заводской практике обычно «короблением»; в) почти достигающими величины сил прочного сцепления частиц металла в наиболее слабых местах — в этом случае происходят явления как бы самопроизвольного растрескивания или раскалывания изделия даже при спокойном хранении его на складе, — подобного рода случаи раскалывания не редки на складах инструмента; наконец, г) превышающими величину сил прочного сцепления частиц металла — тогда образуются немедленно же трещины, разлет изделия на части, откалывание каких-либо частей изделия и т. п.
Присутствие в материале какого-либо изделия скрытых напряжений может быть подтверждено или разрезкой изделия, или снятием части материала обработкой на станках. Например, при вырезке из паровозного бандажа небольшого куска длиной около 10 мм наблюдается часто схождение концов бандажа после вырезки, причем самое расстояние между этими концами уменьшается на 50—60 мм. Затем, при разрезке на части прокатанной полосы рессорной стали, вытачивании небольших образцов для испытания на разрыв и долговременном хранении этих образцов неиспытанными (завод «Красный Путиловец») было замечено через сутки сильное самопроизвольное искривление двух образцов. Искривление это медленно и очень немного возрастало в течение первой недели хранения, затем осталось постоянным и более не изменилось в течение трех лет. Вид искривленных образцов представлен на фиг. 14. Повторение опыта дало те же самые результаты. Опыт этот иллюстрирует характерную черту скрытых напряжений: крайнюю неравномерность их распределения в теле изделия; наряду с частями объема, свободного от скрытых напряжений, где, следовательно, полностью проявляются силы прочности и упругости металла, в изделиях существуют известные центры развития скрытых напряжений, часто превышающих по величине силы упругости металла; внешнее проявление действия этих скрытых напряжений временно сдерживается силами упругости ненапряженных частей металла, удаление которых заставляет немедленно проявить себя имеющимся скрытым напряжениям, изменяющим внешнюю форму металла.
Присутствие в металле скрытых напряжений чрезвычайно сильно влияет на свойства металла в изделиях, а следовательно, служит значительным фактором разнообразия свойств стали одного и того же состава, одного и того же строения, в одном и том же изделии. Особенно важное значение приобретает этот фактор в деле испытания материалов, при установлении доброкачественности стали в изделиях, при самой приемке изделий, изготовленных заводами.
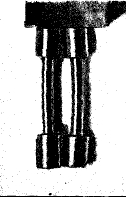
Фиг. 14. Образцы, выточенные из полосы рессорной стали и самопроизвольно изогнувшиеся в течение одной недели.
II. КЛАССИФИКАЦИЯ СОРТОВ стали. В основу классификации сортов стали может быть положен один из следующих двух принципов: 1) назначение стали; 2) состав стали и ее происхождение. Ввиду многочисленности и чрезвычайного разнообразия сортов стали обычно приходится пользоваться и тем, и другим принципами классификации совместно.
1. Классификация сортов стали по назначению. По назначению все сорта стали метальных сплавов могут быть разделены на четыре обширные группы: 1) сталь строительная; 2) машиноподелочная сталь; 3) инструментальная сталь и 4) сталь и стальные сплавы особого назначения.
К первому классу относится сталь мостовая, железнодорожная, балочная всех профилей, судостроительная и т. п. Ко второму классу – осевая, бандажная, рессорная, пружинная подшипниковая, автомобильная, тракторная, аэропланная, артиллерийская, турбинная и т. п. К третьему классу — инструментальная углеродистая, инструментальная специальная, быстрорежущая, штамповая, волочильная, калибровая, ножевая, напильниковая, буровая и т. д. Четвертый класс сталь может быть в свою очередь разделен на многочисленные разряды, главнейшими из которых являются: сталь, сопротивляющаяся изнашиванию; сталь и сплавы, обладающие низкими коэффициентами расширения; сталь и сплавы для постоянных магнитов; сталь и сплавы с большой магнитной проницаемостью; сталь маломагнитная; нержавеющая сталь; сталь и сплавы, не окисляющиеся при нагревании; сталь устойчивая при частых и резких колебаниях температуры и давления.
Каждый разряд подразделяется на более мелкие группы сортов стали, причем основой этого дальнейшего деления служат уже признаки классификации другого рода, т. е. химический состав и происхождение стали.
2. Классификация сортов стали по происхождению и по составу.
По происхождению, в зависимости от примененного способа выплавки, сталь может быть: а) томасовской, выплавленной в конвертерах Томаса (см. железоделательное производство); б) бессемеровской, выплавленной в конвертерах Бессемера; в) мартеновской, выплавленной в больших вращающихся мартеновских печах, работающих непрерывным процессом; г) мартеновской основной, выплавленной на основном поду мартеновских печей; д) мартеновской кислой, выплавленной в мартеновских печах с кислым подом; е) мартеновской, выплавленной в мартеновских печах малого размера; ж) электросталью, выплавленной в электрических сталеплавильных печах; з) тигельной, переплавленной в особых горшках (тигли) в печах специального устройства (тигельные печи).
По качеству (малое содержание газов, вредных примесей, неметаллических включений) наилучшей считается сталь тигельная, самая дорогая по способу изготовления. При известных условиях выплавки с тигельной сталью может конкурировать электросталь, превосходящая по своему качеству мартеновскую сталь. Последняя имеет преимущество перед бессемеровской и томасовской по меньшему содержанию в ней растворенных газов. Наиболее высококачественная мартеновская сталь выплавляется в печах малого размера (менее 10 тонн). Печи, работающие непрерывным процессом, дают сталь, содержащую много кислорода в форме соединений с железом и марганцем и требующую специальных приемов для удаления кислорода из стали, для «раскисления» готовой стали.
Химический состав стали отчасти характеризуется названием сорта стали. При отсутствии особо введенных примесей сталь называют обычно «углеродистой» сталью. Введение хотя бы одной примеси обязательно отмечается в названии стали, изменяющемся соответственно введенной примеси; сюда относятся сорта стали: кремнистая, алюминиевая, медистая, никелевая, кобальтовая, марганцовистая, хромовая, ванадиевая, циркониевая, молибденовая, титановая, вольфрамовая, урановая.
При введении в сталь двух примесей название стали делается составным, так как в нем отмечаются обе введенные примеси, главнейшие сорта стали с двумя примесями, особо введенными: кремненикелевая, кремне-марганцовистая, марганцово-никелевая, кремне-хромовая, хромо-медистая, хромо-никелевая, никель-молибденовая, вольфрамо-никелевая, хромо-кобальтовая, хромо-марганцовистая, хромо-ванадиевая, хромомолибденовая, хромовольфрамовая, как показывает перечень названий сортов стали с двумя специально введенными примесями, наиболее распространенной примесью здесь является, несомненно, хром.
В стали может быть введено также и три специальные примеси. Тогда название стали либо составляется из названия всех трех введенных примесей, либо дается более краткое название (марка), независимое от наименования примесей. К числу таких сортов стали относятся; кремне-никель-молибденовая, хромо-никель-марганцовистая, хромо-никель-ванадиевая, хромо-никель-цирконовая, хромо-никель-молибденовая, хромо-никель-вольфрамовая, хромо-кобальт-марганцовистая, хромо-кобальт-вольфрамовая, хромо-ванадий-молибденовая, хромо-вольфрамо-ванадиевая, хромо-вольфрамо-молибденовая. При введении в сталь более трех специальных примесей практикуется обычно называть сталь каким либо сокращенным названием, часто независящим от наименования введенных примесей.
Попытки установления некоторой закономерной последовательности при составлении названия стали с двумя или тремя специальными примесями успехом не увенчались, практически сложное название стали вырабатывается в большинстве случаев фонетически, по удобству произношения. Кроме того, если условиться ставить всегда впереди название примеси, содержание которой в стали является наибольшим, то при таком порядке составления названий общее число названий сортов стали по меньшей мере удвоилось бы, так как наряду с хромовольфрамовой сталью существовала бы, например, сталь вольфрамо-хромовая и т. п.
Все же количественное содержание той или другой примеси должно быть учитываемо при классификации стали; оно отмечается обычно присоединением к названию стали слов: «мало», «средне», «много», «высоко». Так, например, углеродистая сталь с малым содержанием углерода называется малоуглеродистой, при среднем содержании углерода — среднеуглеродистой, при высоком содержании углерода — высокоуглеродистой.
Сталь с большим содержанием марганца носит название «высокомарганцовистой», с большим содержанием хрома — «высокохромовой». Даже при двойных названиях стали в некоторых странах применяется иногда количественная отметка содержания примеси; так, в работах американского Burean of Standards отдельные сорта быстрорежущей стали называются: высоковольфрамовые-малованадиевые, маловольфрамовые-высокованадиевые и т. п.
III. СПЕЦИАЛЬНАЯ СТАЛЬ И СТАЛЬНЫЕ СПЛАВЫ. При содержании в стали каких-либо иных примесей, кроме обычно получающихся при заводском изготовлении стали (марганец, кремний), или при значительно повышенном против обычной нормы содержании постоянных спутников железа — марганца и кремния, сталь получает название — на английском языке — Alloy Steel (стальной сплав); аналогичные названия применяют также в Италии и Испании; на немецком языке — legiertes Stahl (стальной сплав), или Sonderstahl (особая сталь, устарелое название), или же при наличии особо выдающихся свойств также Edelstahl (благородная сталь); на французском языке — l’acier special (специальная сталь) и, наконец, на русском языке — специальная сталь. Последний термин «специальная сталь», применяемый также в Швеции, Дании и Голландии, в немецком языке имеет совсем особое значение: в Германии специальной сталью называют всякую сталь, изготовляемую для определенного назначения.
Вводимые в сталь примеси ведут себя различно по отношению к железу, как основной составной части стали, и к углероду, постоянной и неизбежней примеси стали.
По отношению к железу при введении добавочной примеси мыслимы две возможности: 1) образование твердого раствора введенного элемента в железе, 2) образование определенного соединения примеси и железа. В последнем случае возможно или устойчивое существование определенного соединения и полное не смешивание его с железом при известных температурных условиях, или же сравнительно легкая разложимость соединения и переход распавшейся части соединения в твердый раствор.
По отношению к углероду примеси, вводимые в сталь, могут быть либо совершенно индифферентными, либо обладающими некоторым слабым сравнительно стремлением к образованию соединения с углеродом, путем вытеснения части железных атомов из карбида железа, либо обладающими столь сильным стремлением к образованию соединения с углеродом, что существование карбида железа становится невозможным ввиду насыщения всех атомов углерода атомами введенной примеси. Далее, количественное соотношение введенного элемента и углерода в образовавшемся карбиде может быть различным в зависимости от температурных условий, другими словами, для некоторых примесей существует несколько форм карбидов, обладающих устойчивостью в различных температурных областях (хром).
В течение послевоенного десятилетия теоретическая металлургия чрезвычайно обогатилась, приобретя совершенно новый метод изучения природы металлов и их физического строения вплоть до расположения отдельных атомов в правильные решетки, определяющие собой форму кристаллов каждого отдельного металла. Этот метод — рентгенографическое изучение строения металлов, — давая возможность изучать построение атомных кристаллических решеток, позволил несколько ориентироваться в вопросе о поведении примесей в специальной стали. Для этого необходимо ознакомиться с формами кристаллических решеток, как самого железа, так и всех технически важных спутников его в стальных сплавах.
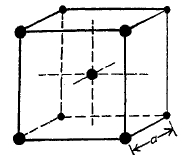
Фиг. 15. Схематическое строение атомной кристаллической решетки α-железа.
Как известно, железо (см. XX, 145) при нагревании, оставаясь в твердом состоянии, испытывает аллотропические превращения, резко изменяющие все свойства металла. Более или менее твердо установленных аллотропических форм железа известно четыре: железо-α, свойства которого хорошо всем известны, так как эта форма является обычной формой железа при атмосферной температуре. Таковым железо сохраняется при нагревании до 769°С, после чего переходит в аллотропическую форму β, чрезвычайно слабо магнитную. При температуре 906° β-железо переходит в γ-железо, совершенно немагнитную форму, отличающуюся от α-железа также и по удельному весу, и удельному объему. При температуре приблизительно 1400°С совершается дальнейший переход железа из γ формы в форму сравнительно мало изученную и практически трудно достижимую.
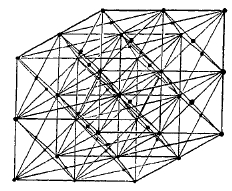
Фиг. 16. Схематическое строение атомной кристаллической решетки γ-железа (W. Rosenhain).
Как и следовало ожидать, кристаллические решетки различных аллотропических форм железа оказались различными. Для железа-α решетка может быть представлена как бы состоящей из кубиков правильной формы с одним атомом в центре и восемью по вершинам трехгранных улов кубика — такая форма решетки, изображенная на фиг. 15, носит название «кубической пространственно центрированной» решетки. Совсем другой вид имеет решетка другой главнейшей аллотропической формы железа, устойчивой в области температур выше 906° — так называемого γ-железа. Основной формой решетки здесь является также куб, но не с одним атомом в центре таковой в решетке γ-железа отсутствует, а с добавочными атомами, расположенными в центрах граней куба; остальные 8 атомов, так же как и у α-железа, могут быть представлены расположенными по вершинам трехгранных углов куба. Вся решетка γ-железа (фиг. 16) может быть представлена состоящей из элементарных кубиков, подобных изображенному на фиг. 17 и носящих название «куб с центрированными поверхностями».
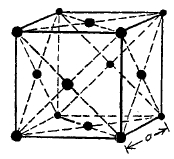
Фиг. 17. Элементарный кубик решетки с центрированными поверхностями.
Что же касается решеток β и δ железа, то и та и другая предполагаются на основании работ Westgreen'а подобными решеткам α-железа. Существует весьма вероятное предположение Ваіn'а, Boylston'а и др. исследователей, подкрепленное работой Fink'a и Campbell’a, относительно некоторых отличий решетки β-железа от решетки α-железа. Fink вообще констатировал, хотя и не на основании вполне достоверного материала, что в закаленной стали существует решетка с исходной формой тетрагональной призмы. Bain предположительно выявил переходную форму решетки между γ и α-желеэом (см. фиг. 18), имеющую вид тетрагональной призмы. Boylston предположил, что тетрагональная решетка — есть форма строения β-железа.
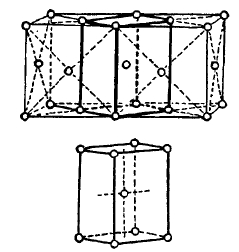
Фиг. 18. Строение решетки формы между α и γ-железом (E. C. Bain).
Таблица 3.
Физические свойства главнейших образующих сталь элементов (по Z. Jeffries и R. S. Archer).
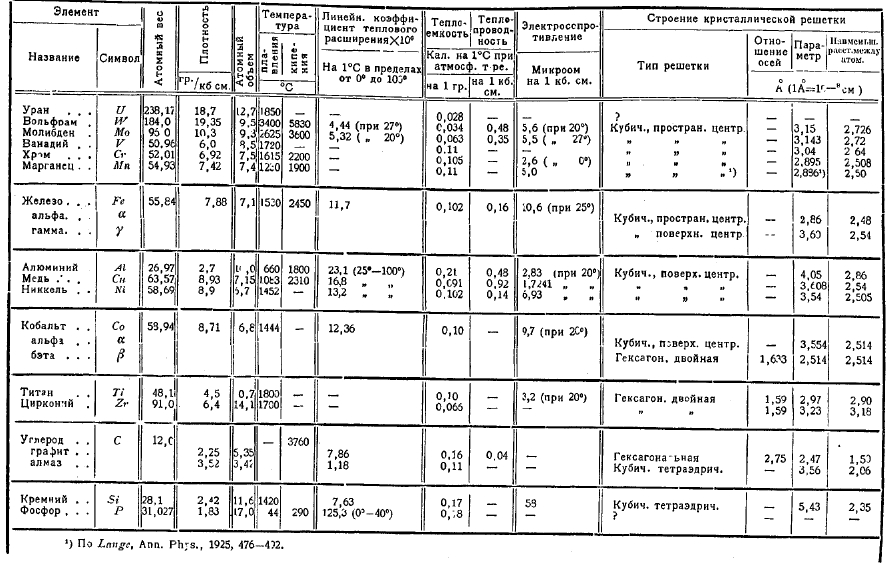
По своему атомно-кристаллическому строению все вводимые в сталь добавочные «специальные» элементы (см. табл. 3) могут быть отнесены к следующим группам: 1) решетка кубическая сцентрированными гранями, сюда относятся: Сu, АІ, α- и β-Ni, α-Co; 2) решетка кубическая пространственно центрированная — сюда принадлежат: Cr, V, Mo, W; 3) решетка в форме тетраэдрических кубиков: углерод—алмаз и кремний; 4) гексагональная решетка—графит; 5) двойная — гексагональная: β-кобальт, титан и цирконий. В перечне не указаны два элемента, — марганец и уран: решетка последнего еще не установлена, об решетке первого не имеется отчетливого представления; G. Tammann приписывает марганцу решетку первой группы, H. Lange — решетку второй группы, А. Westgreen и G. Phragmen — также решетку первой группы для α-Мn. G. Tammann считает также и ванадий образующим решетку первой группы с центрированными гранями куба.
Непрерывные твердые растворы могут легко образовывать такие два элемента, решетки которых аналогичны по строению и близки по основным размерам. Такими элементами можно считать: α-Fе и Mn, α-Fe и Сr, γ-Fe и β-Ni, γ-Fe и α-Ni, γ-Fe и Сu. По отношению к α-Fe все элементы первой группы обладают также способностью давать твердые растворы, но до известной предельной концентрации. Другой характерной особенностью элементов I группы является то обстоятельство, что все они не дают более или менее устойчивых соединений с углеродом. Таким образом, введение в сталь одного из элементов Сu, АІ, Ni или α-Со может влиять лишь на свойства основной массы железа, заменяя его образующимися твердыми растворами, и совсем не оказывает влияния на свойства имеющихся в сталь образований карбида железа (цементит). Может быть отмечено в этом отношении влияние алюминия, стремящегося при достаточно высоком содержании его в растворе совершенно оттеснить карбид в область с меньшей концентрацией алюминия (фиг. 19).
Фиг. 19. Строение стали с местным высоким содержанием Al.
Наиболее важной технически примесью стали этой группы элементов является никель.
Вторая группа примесей стали, обладающая решеткой кубической, пространственно центрированной – подобной решетке α-железа (фиг. 16) – Cr, V, Mo, W, - в противоположность первой группе, все дают прочные соединения с углеродом: карбиды хрома, ванадия, молибдена, вольфрама; при этом стремление их к соединению с углеродом столь велико, что при достаточном содержании примеси из соединения с углеродом вытесняется все железо, и карбид железа перестает существовать, уступая место карбидам специальных примесей. По отношению к α-железу примеси эти обладают также способностью растворяться и образовывать твердые растворы; эта способность постепенно ослабляется по мере увеличения атомного номера элемента, в то время, как стремление к соединению с углеродом, наоборот, возрастает с возрастанием атомного номера. Есть основания предполагать, что примеси, действуя одновременно и на пластическую составляющую стали, железо, и на твердую составляющую - карбид, чрезвычайно сильно изменяют свойства стали, делая их разительно несхожими со свойствами сталь обыкновенной, не содержащей специальных примесей. Достаточно указать на такие замечательные сорта стали, как нержавеющая сталь с высоким содержанием хрома, быстрорежущая сталь с высоким содержанием вольфрама, хрома и ванадия.
К третьей группе примесей относятся элементы со сложной кубической решеткой, построенной как бы из двух решеток, входящих одна в другую таким образом, что вершины тетраэдров одной решетки располагаются посредине граней тетраэдров второй решетки (G. Tammann). Таковым строением обладают углерод-алмаз и кремний (рис. 20). Предположение о том, что углерод в стали может являться в форме алмаза (А. А. Байков) не доказано экспериментально. Некоторое сходство решетки этой группы с решеткой γ-железа (поверхностно центрированный куб) хорошо согласуется со способностью углерода растворяться до известного предела именно в γ-железе. С α-железом углерод образует, как указывалось выше, прочное определенное соединение Fе3С, карбид железа.
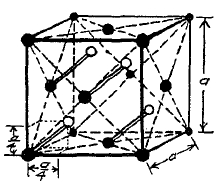
Фиг. 20. Тетраэдрическая кубическая решетка кристаллов алмаза и кремния (L. W. Mс. Kechan и E. C. Bain).
Кремний также дает соединение с α-железом — силицид железа Fe2Si2 (Murakami, Курнаков), распадающееся при переходе железа в форму γ-железа. Кремний обладает большей растворимостью в γ-железе, чем в α-железе.
Четвертая группа. Углерод-графит, имеющий гексагональную решетку совершенно особенной формы с отношением высоты к стороне шестиугольника равным 2,75, всегда находится самостоятельно существующим в α-железе, но с γ-железом образует твердый раствор, предельная концентрация которого приблизительно совпадает с предельной концентрацией растворимости в γ-железе другой формы углерода, освобождающейся при разложении железного карбида. Как составляющая стали графит всегда нежелателен, так как его присутствие неизбежно ослабляет сталь, образуя места с пониженными силами сцепления частиц.
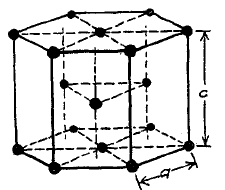
Фиг. 21. Двойная гексагональная решетка кристаллов титана, кобальта и циркония (L. W. Mс. Kechan и E. C. Bain).
Пятая группа примесей, имеющая двойную гексагональную решетку (фиг. 21) — β кобальт, титан и цирконий — является группой малоизученной. Но все же можно констатировать, что некоторые из этих примесей, в особенности же кобальт, оказывают чрезвычайно сильное влияние на отдельные свойства стали (задерживательная сила при намагничивании).
Марганец, по характеру своего влияния на свойства стали, чрезвычайно сильного и резкого, скорее всего, может быть поставлен в ту же группу, как и хром, т. е. с пространственно центрированной решеткой. Он способен давать определенное соединение с углеродом Mn3С, карбид марганца, обладает достаточною растворимостью в α-железе и, по-видимому, меньшей способностью растворяться в γ-железе. Прибавление к стали 12% Мn делает сталь нестирающейся (высокомарганцовистая сталь Гадфильда).
Принимая во внимание разнообразие взаимоотношений каждой отдельной примеси с основными строительными материалами стали — железом и карбидом железа, можно понять стремления металлургов к одновременному использованию влияния нескольких примесей из одной и той же или из различных групп, охарактеризованных выше.
Главнейшие и наиболее распространенные сорта специальной стали перечислены в последней главе настоящей статьи.
IV. ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ. К временам глубокой древности относится открытие замечательного свойства сталь «принимать закалку», «закаливаться». Изобретательность человека сумела использовать это свойство для своих целей, как созидательных (инструменты), так и разрушительных (орудия войны). Еще несколько десятилетий тому назад существовал общепонятный простой взгляд на сталь и ее свойство закаливаться: сталь — это материал прочный, обладающий вполне определенными свойствами, всегда одинаковыми; закаленная сталь — синоним большой твердости, упругости, неподатливости. По мере углубления наших знаний в изучение природы, в эпоху огромного расцвета физики в первой четверти XX столетия, взгляд на природу стали и ее способность закаливаться все более и более усложнялся, существовавшая некогда ясность все более и более затушевывалась. Но это отсутствие ясности лишь предрассветный туман: годы упорной работы, как лабораторной, так и философски-обобщающей, не прошли бесследно — плоды многолетних трудов ученых, исследователей и металлургов дают возможность наметить хотя бы в общих чертах определенную теорию закалки стали.
Основой этой теории является принцип изменяемости свойств стали в связи с изменяемостью ее физического строения.
Факторами, влияющими на изменение строения стали, являются: 1) температура, 2) работа внешних сил, 3) время. Несомненно, сильнейший из этих факторов — температура, т. е. изменение теплового состояния стали.
При нагревании стали, при достижении известной скорости тепловых колебаний частиц происходят в стали внезапные явления, протекающие с чрезвычайно большой скоростью. Эти явления в основных чертах сводятся к следующему: а) происходит перестройка кристаллической решетки, меняющей одновременно или в чрезвычайно близкой последовательности как самую форму расположения атомов, так и расстояние между атомами; б) как следствие первого явления — происходит резкое и внезапное изменение объема стали, связанное с выделением некоторого количества теплоты; в) вследствие перестройки кристаллической решетки нарушаются существовавшие до этого момента взаимоотношения между отдельными веществами, участвующими в построении рассматриваемого объема стали, в результате чего получается после превращения совершенно новое строение с новым расположением не только атомов железа, но также атомов других элементов, входящих в состав стали; сравнительно просто объясняется то, что происходит при этом с атомами углерода: до перестройки решетки железа из формы α- в форму γ углерод существовал в стали, соединенный с тройным количеством атомов железа, образуя легко видимое и различимое в микроскоп тело — карбид железа; после же перехода железа в форму γ непосредственное изучение строения стали не дает возможности установить присутствия какого-либо, отличимого от общей массы, тела; карбида, как отдельной составляющей, более не существует, составлявшие его атомы железа и углерода приняли участие в построении общей однородной массы стали: железо — как материал для построения решетки, углерод — как вещество растворенное, атомы которого располагаются внутри решетки основного тела.
Таким образом, некоторый незначительный импульс в виде ничтожного ускорения тепловых колебаний влечет за собой целую цепь превращений первостепенного значения, превращений, приводящих к полному изменению строения и природы имевшегося металла.
При обратном изменении теплового состояния, при постепенном замедлении тепловых колебаний, обычно, с очень редкими и немногими исключениями, возникает также в определенный момент, при определенной скорости тепловых колебаний, импульс к восстановлению прежнего состояния. Повторяются снова процессы, происходившие при нагревании: внезапно перестраивается решетка из формы γ в форму α, происходит связанное с этой перестройкой изменение объема стали, атомы углерода и др. элементов, растворенные в у-железе, не имея более возможности оставаться в новой решетке, вновь возвращаются к самостоятельному существованию, связываясь с соответствующим количеством атомов железам объединяясь в структурные формы; различимые глазом в микроскоп при достаточном увеличении.
Несомненно, при такой сложности и многообразии происходящих совместно явлений вероятность получения после нагревания и охлаждения строения, тождественного с имевшимся первоначально, до нагревания, — ничтожно мала, почти всегда получатся некоторые новые формы взаимного расположения отдельных структурных составляющих стали.
Но изменение строения равнозначаще изменению свойств, как функции строения. Этим соображением легко объясняется легкость изменения свойств стали.
Второе основное положение теории закалки стали может быть формулировано следующим образом. Конечное состояние стали (комплекс: строение и свойства) после охлаждения в сильной степени зависит от скорости изменения теплового состояния стали при охлаждении.
Процессы, происходящие в стали при охлаждении, являясь по самой природе своей функцией изменения расположения и перемещения атомов, самым тесным образом связаны с интенсивностью теплового состояния тела; для возможности протекания этих процессов необходимы вполне определенные пределы изменения скорости тепловых колебаний: выйдя из этих пределов в сторону уменьшения скорости колебаний, неизбежно встретимся с явлением замедления и даже полной задержки процессов изменения расположения атомов.
При охлаждении нагретого металла должна существовать некоторая строго ограниченная область тепловых состояний, дающая возможность протекать всему ряду процессов, описанных выше. Область эта начинается с момента возникновения первого импульса к превращению и заканчивается некоторой вполне определенной скоростью тепловых колебаний (температурой), при которой становится чрезвычайно затрудненным перемещение атомов.
Каждое отдельное превращение в некотором объеме совершается полностью в течение известного промежутка времени τ1, для следующего за ним превращения требуется время τ2 и т. д. С другой стороны, охлаждение стали может быть выполнено практически с любой скоростью в пределах от весьма быстрого охлаждения, например, в жидком воздухе, до весьма медленного охлаждения, — в печи, остывающей с подтапливанием; следовательно, то время — Θ, в течение которого металл при охлаждении пребывает в области тепловых состояний, допускающих превращения, может изменяться в пределах достаточно широких. Рассматривая соотношение между Στ, т. е. суммарной продолжительностью всех совершающихся в стали при охлаждении процессов, и Θ — временем охлаждения от начальной температуры превращения до температуры полной задержки превращений, можно допустить возможность трех отдельных случаев: 1) Q>Στ (медленное охлаждение), 2) Q=Στ и 3) Q<Στ (быстрое охлаждение). Несомненно, конечное состояние стали после охлаждения будет резко различным во всех этих трех случаях. Если считать нормальным первый случай, приводящий ко вполне устойчивому состоянию законченных превращений, то во втором случае будет наблюдаться некоторая незаконченность последних стадий превращения, в третьем же случае — полная задержка последних стадий или даже всего ряда превращений.
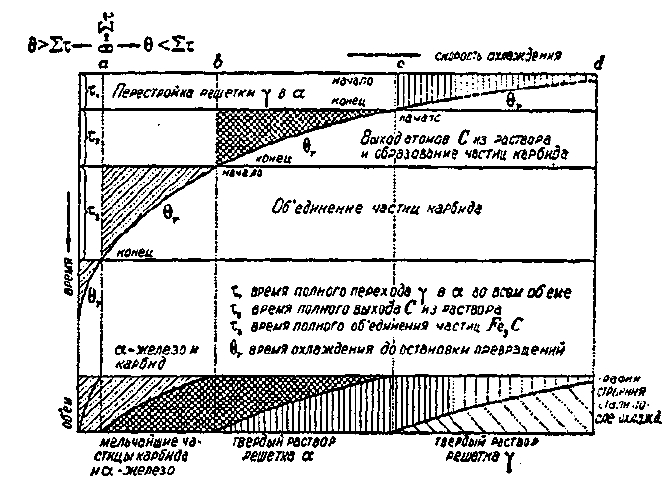
Фиг. 22. Диаграмма, выражающая зависимость меду скоростью охлаждении стали и ее конечным строением после охлаждения (Н. Т. Гудцов).
В общем случае, предполагая непрерывность изменения Θ, — времени охлаждения некоторого малого объема до теплового состояния, фиксирующего расположение атомов, характер влияния соотношения Στ и Θ на конечное строение металла может быть выражен диаграммой, разработанной Н. Гудцовым («Курс лекций по термической обработке стали) и изображенной на фиг. 22. Эта диаграмма дает возможность установить следующие положения:
I. Постепенно уменьшая Θ можно последовательно задерживать процессы: 1) объединения образовавшихся при перестройке кристаллической решетки частиц карбида железа (от а до b на фиг. 22); 2) выхода из решетки железа атомов углерода и др. элементов (от b до с); 3) превращения решетки γ-железа в решетку α-железа (от с до d).
II. Существование однотипного строения в каждом мельчайшем объеме стали является случаем, вероятность получения которого сравнительно очень мала (случаи а, b, с и d на фиг. 22).
III. Наиболее частым и общим случаем строения стали при скоростях охлаждения, соответствующих Q<Στ, т. е. быстрому охлаждению, является совместное существование в каждом мельчайшем объеме конечных стадий двух смежных по времени процессов, — последующего и предыдущего — см. график строения стали после охлаждения внизу диаграммы фиг. 22.
Три основные формы строения стали, получаемые при быстром охлаждении: а) распавшегося твердого раствора, б) пересыщенного твердого раствора в α-железе, в) нормального твердого раствора в γ-железе, — отличаются одна от другой значительною разностью физических своих свойств. Одним из наиболее существенных обстоятельств служит наблюдаемое различие удельных объемов всех трех перечисленных форм строения стали, причем различие это по границе перехода твердого раствора γ-железа в твердый раствор α-железа более значительно. При вероятности частого получения при закалке строения, комбинированного из двух, различных соседних форм строения, особо важное значение получает существование различия в удельных объемах. Это различие неизбежно влечет за собой возникновение в быстро охлажденном металле скрытых напряжений большой сравнительно величины, способных повлечь за собой растрескивание изделия или же сильное коробление его. Особенно опасна в этом отношении область, лежащая непосредственно вправо от ординаты с на диаграмме фиг. 22.
Наблюдаемые на практике случаи растрескивания закаливаемых изделий при незначительном повышении температуры закалки на несколько градусов хорошо объясняются графиком строения быстро охлажденной стали: повышение температуры закалки, как известно, равносильно повышению скорости охлаждения, перемещение же скорости охлаждения изделия вправо (фиг. 22) может повлечь за собой сохранение в каждом мельчайшем объеме некоторого незначительного, может быть, количества решетки γ-железа, присутствие каковой в окружении решетки α-железа способно вызвать громадные скрытые напряжения, разрушающие изделие.
Таким образом, мы приходим к общему выводу из всего сказанного о строении стали при быстром охлаждении: применяя различные скорости охлаждения стали, нагретой до температуры, лежащей выше точки превращения альфа-железа в гамма-железо, в общем случае мы всегда получаем комбинированное строение стали, состоящей из а) твердого раствора углерода в альфа-железе и б) либо распавшегося твердого раствора, либо твердого раствора углерода в гамма-железе; при этом количественное соотношение той и другой формы строения в данном объеме изменяется в зависимости от скорости охлаждения в пределах от 0 до 100%. Совместное существование различных форм строения стали неизбежно связывается с развитием в металле скрытых напряжений большей или меньшей величины.
2. Свойства стали, соответствующие различным формам строения, получаемых при быстром охлаждении. Наиболее замечательны сами по себе и наиболее отличны от свойств обычной стали — свойства стали, охлажденной с такой скоростью, при которой основной формой строения является твердый раствор углерода в альфа-железе. Закаленная сталь, имеющая однородное строение этого твердого раствора при достаточной концентрации углерода (>0,5%), может быть рассматриваема, как тело чрезвычайно твердое, совершенно упругое, не выдерживающее никакой пластической деформации и совершенно хрупкое, ломающееся внезапно без предварительного смещения (перетекания) частиц, при нагрузках случайных, в сильной степени зависящих от величины внутренних напряжений в закаленной стали. Так, закаленные образцы, например, рессорной стали, вырезанные из одного и того же куска стали, разрушались при испытании: одна образец при 60 кг/кв. мм (сильные внутренние напряжения), второй образец при 180 кг/кв. мм (незначительные по величине внутренние напряжения) Трудно получаемое для обыкновенной стали строение с преобладающей формой твердого раствора в гамма-железе связывается обычное сильным понижением магнитных свойств стали — в конечном итоге, при получении сплошного строения решетки гамма-железа сталь становится совершенно немагнитной. В отношении механических свойств такая сталь является материалом средней твердости, вязким, недостаточно упругим.
Сталь, имеющая преимущественное строение распевшегося раствора с чрезвычайно мелким распределением образовавшихся при распадении раствора частиц карбида железа, отличается от обычной стали своей повышенной твердостью, повышенной прочностью, хорошим сопротивлением износу и истиранию.
Возникает вопрос, какая же из форм строения, получаемых при быстром охлаждении стали, представляется технически наиболее желательной? Пользуясь методам исключения формы, заведомо непригодной, хрупкой, и формы, практически недостижимой для обыкновенной стали без специальных примесей, приходим к выводу, что наивыгоднейшей из трех является форма строения распавшегося раствора.
Но, как указывалось выше, получение такой формы строения стали путем одного только быстрого или ускоренного охлаждения — задача чрезвычайно гадательная; малейшее изменение условий охлаждения влечет за собой получение некоторого избытка соседних форм, т. е. заметной степени дифференциации распавшегося раствора, с одной стороны, твердого раствора в альфа-железе — с другой стороны.
Поэтому, металлургическая практика, значительно опередив теоретическое обоснование процессов термической обработки, нашла иной путь получении наивыгоднейшего строения стали. Этот путь заключается в перемене самого направления изменения теплового состояния: вместо фиксирования известного строения стали при определенной скорости охлаждения более практичным оказалось получение аналогичного же строения при вторичном нагревании стали, предварительно охлажденной настолько быстро, чтобы сохранилось строение действительного твердого раствора углерода в альфа-железе. Нагревая сталь, сохранившую строение твердого раствора, постепенно и осторожно, получаем возможность; 1) создать условия для прохождения того процесса выхода атомов углерода из раствора и образования частиц карбида, который был задержан благодаря быстрому охлаждению; 2) регулировать самый процесс распадения твердого раствора и объединения частиц карбида — останавливая нагревание на известной температуре, соответствующей желательной для нас степени развития процесса. При таком способе придания стали наивыгоднейшего и наиболее однородного строения легко может быть достигнута цель, недостижимая почти при использовании только одного охлаждения стали без последующего нагревания. Испытание механических свойств стали, обработанной подобным образом со вторичным нагреванием после быстрого охлаждения, подтверждает все вышесказанное. Действительно, свойства стали изменяются все время, следуя за изменением температуры нагрева стали после закалки. При малых степенях «отпуска» — так называетс эта операция на практике, — получается материал с высокими упругими свойствами (влияние свойств твердого раствора), но недостаточным запасом пластичности. Дальнейшее повышение температуры отпуска влечет за собой постепенное понижение упругих свойств и соответствующее возрастание свойств пластических. При такой температуре нагрева сталь при отпуске, при которой частицы карбида получают возможность более или менее свободно перемещаться, а также при достаточно продолжительной выдержке при этой температуре, получаем свойства, близкие к свойствам стали, имевшимся первоначально, до термической обработки, но заметно «улучшенные», благодаря чему и самая операция получила название в Германии «Vergüten» — улучшения.
Таким образом, термическая обработка (тепловая) стали должна составляться, в общем случае, из двух совершенно отдельных операций: 1) закалки, т. е. нагрева до температур, достаточно высоких для того, чтобы в стали все железо перешло в форму гамма-железа, и быстрого охлаждения от этой температуры, с целью получения преимущественной формы строения твердого раствора углерода в альфа-железе, и 2) отпуска — нагрева до температур сравнительно низких (от 150° до 650°С), с целью получения однородного строения распавшегося твердого раствора с различной степенью дифференциации продуктов распадения раствора.
3. Наклеп стали (холодная механическая обработка давлением). Подобного же рода изменение свойств стали, как и при термической обработке, может быть достигнуто путем известной степени деформирования куска стали в холодном состоянии. При этом в особенности для малоуглеродистой стали наблюдается значительное повышение упругих свойств и понижение свойств пластических. Примером может служить волочение проволоки которым достигается повышение упругости стали в 5—6 раз при соответствующем падении пластических свойств. Механизм воздействия наклепа на строение и свойства стали недостаточно изучен.
4. Отжиг стали. Переходя к области обычного охлаждения стали, соответствующего условиям Θ = Στ и Q>Στ (см. диаграмму фиг. 22), мы снова сталкиваемся с возможностью получения неоднородного строения стали, являющегося в этом случае следствием двух причин: 1) получения различной степени роста образований карбида железа в разных областях изделия, 2) получения различной величины зерна (кристаллических областей с одинаковой ориентировкой осей) структурных составляющих стали. И то, и другое обстоятельство влечет за собой изменение свойств стали в худшую или лучшую сторону.
Практически возможны два случая: во-первых, когда изделие, изготовленное из стали, применяется без дальнейшей термической обработки; во-вторых, когда изготовленное изделие подвергается, с целью получения наивыгоднейших свойств, термической обработке. В том и другом случае представляется необходимым придать металлу известную степень однородности строения и свойств, что и достигается путем применения операции тепловой обработки, состоящей из нагревания до известной температуры и последующего спокойного охлаждения более или менее замедленного. Подобного рода операции тепловой обработки носят название: «отжига» (Annealing, recuit, Glühen) при охлаждении достаточно медленном, «нормализации» (normalisation) при охлаждении в атмосферном воздухе, «отжига при низких температурах» (Ionnealing), если температура нагрева не превышает температуры превращения, совершающегося в стали при нагревании.
Отжиг, как предварительная операция, подготовляющая сталь к дальнейшей термической обработке, выполняется так, чтобы металл получил наибольшую мягкость и наибольшую вязкость, соответствующую наиболее равномерному и мелкому распределению структурных составляющих стали. Отжиг, как окончательная операция, выполняется несколько иначе, учитывая то обстоятельство, что свойства материала должны проявить себя в безболезненной и долговременной работе изделия. В этом случае вырабатывается некоторая вполне определенная последовательность скоростей охлаждения стали, соответствующая получению равномерного строения и несколько повышенных упругих свойств.
В том и другом случае температура нагрева выбирается немного превышающей температуру превращения альфа-железа в гамма-железо.
5. Обработка поверхностного слоя стальных изделий. Во многих случаях практики машиностроения приходится, с целью наибольшего использования стали, как машиностроительного материала, прибегать к таким способам обработки стали, которые позволили бы нам получить сочетание в одном и том же изделии совершенно различных свойств металла. Так, например, при изготовлении автомобильных шестерен необходимо, чтобы материал трущихся поверхностей зубцов обладал наиболее высокой твердостью и способностью сопротивляться истиранию, в то же самое время внутри шестерни, претерпевающей в работе очень большие напряжения под действием сил постоянных и мгновенных (удары), металл должен иметь значительную вязкость, однородность строения, при достаточно высоком сопротивлении ударам.
Задача сочетания различных, часто даже взаимно исключающих свойств в одном и том же куске металла решается практически различными путями: 1) применением соответственно разработанных и видоизмененных условий термической обработки, 2) применением совершенно особых операций обработки, связанных с изменением химического состава отдельных слоев металла.
В первом случае применяются такие способы нагревания стали, которые дают возможность получать температуру, необходимую для закалки лишь в некотором слое металла, более или менее глубоком, внутри же металл должен иметь более низкую температуру, недостаточную для закалки. Подвергая быстрому охлаждению нагретое таким образом изделие, получают в результате известную степень закаленного состояния в поверхностном слое, постепенно переходящего в состояние незакаленное во внутренних областях изделия. Применение этого способа обработки возможно лишь в очень хорошо оборудованных термических мастерских с хорошо регулированными печами при точном измерении температуры рабочего пространства печи, поверхности нагреваемого изделия, закалочной ванны, а также при точном измерении времени выдержки изделия в печи. В обычных же условиях работы способ этот не применим.
При обработке поверхностного слоя металла с изменением его химического состава используется явление диффузии, т. е. способности атомов одного тела распространяться среди кристаллических решеток другого тела; явление диффузии может быть использовано во всех тех случаях, когда вводимое тело обладает стремлением к растворению в основном теле, но и в случае отсутствия этого стремления можно осуществить распространение атомов при том условии, что оба эти тела способны давать какие-либо определенные соединения — в этом случае играет роль особая разновидность диффузии — «диффузия реакций».
Практическое осуществление получили следующие способы обработки поверхности стальных изделий:
а) цементация, насыщение поверхностного слоя сталь углеродом; б) нитрирование, насыщение поверхностного слоя сталь азотом; в) алитирование, насыщение поверхностного слоя стали алюминием.
Цементация стальных изделий требует для своего выполнения: известной среды, окружающей металл и способной отдавать свой углерод стали, известных температурных условий, известной продолжительности во времени. Наиболее подходящей для отдачи углерода металлу средой является смесь газов СО и СО2; освобождающейся при диссоциации СО, протекающей по известному уравнению 2 СО = СО2 + С, углерод поглощается железом, переходя в твердый раствор, концентрация атомов углерода в котором, будет на поверхности все время повышаться до тех пор, пока не достигнет своей предельной величины, определяемой температурой нагрева металла.
Обычно, для генерации газовой среды вокруг обрабатываемого изделия применяется смесь хорошего древесного угля (березового) с углекислыми солями какого-либо из металлов: калия, натрия или бария.
Температурные условия цементации устанавливаются на основании следующих соображений: 1) сталь должна быть нагрета до такого состояния, которое вполне обеспечивало бы возможность растворения углерода в железе, другими словами, все железо в стали должно находиться в форме гамма-железа; 2) принимая во внимание необходимость осуществления явления диффузии атомов углерода от поверхностного слоя вглубь металла, при выборе температуры следует руководствоваться также зависимостью скорости диффузии углерода в железе от температуры.
При рационально установленной температуре цементации, которая при обработке малоуглеродистой стали приближается к 900°—950°, должно установиться известное закономерное соотношение между скоростями двух процессов, составляющих сущность операции: процессом накопления атомов углерода на поверхности металла, с одной стороны, и процессом диффузии атомов углерода вглубь от поверхности — с другой стороны. В случае слишком малой скорости диффузии (недостаточная температура, недостаточная продолжительность выдержки при нагреве, слишком быстрое нагревание) наблюдается повышенная концентрация углерода на поверхности и слишком резкий переход от цементованного слоя к основному металлу, благодаря чему цементованный слой становится непрочно сидящим на изделии и легко дает откалывание отдельных частей наподобие скорлупы. Наоборот, при слишком быстрой диффузии (чрезмерная температура нагрева) наблюдается другая крайность — недостаточное содержание углерода в поверхностном слое, а, следовательно, и недостаточная твердость поверхности после закалки цементованного изделия. И тот, и другой недостаток легко устраняются соответствующим подбором температурных условий в каждом отдельном случае выполнения цементации.
Продолжительность операции являемся величиной, зависящей от требующейся глубины цементованного слоя и определяется в конечном счете скоростью диффузии при заданных температурных условиях. Наиболее распространенным случаем является получение глубины цементованного слоя около 1 мм, достигаемой при продолжительности операции 2—3 часа.
Само собой разумеется, что введение углерода в поверхностный слой стали имеет смысл только в том случае, когда в обрабатываемом металле содержание углерода достаточно мало.
После насыщения поверхностного слоя металла углеродом производится обязательно полная термическая обработка изделия, причем условия этой обработки вырабатываются таким образом, чтобы в первую очередь было придано желательное строение малоуглеродистому сердечнику и затем уже дополнительными операциями, производимыми при более низких температурах, придают необходимое строение, и свойства поверхностному слою.
б) Нитрирование стальных изделий разработано лабораторией заводов Круппа в Германии. Основой этого процесса является введение избыточного азота в поверхностный слой стали, получение определенного соединения азота с железом, нитрида железа, и твердого раствора азота в железе-альфа. Результатом операции является чрезвычайное возрастание твердости обрабатываемого слоя. Преимущества перед цементацией — отсутствие необходимости производить после нитрирования термическую обработку изделия, связанную с изменением размеров, короблением и растрескиванием изделия.
в) Алитирование, или насыщение поверхностного слоя стали алюминием — также процесс, разработанный лабораторией заводов Круппа в Германии. Основой процесса является образование на поверхности твердого раствора железа в алюминии, обладающего весьма ценным практическим свойством — устойчивостью от окисления при нагреве до высоких температур. Обработанные алитированием изделия оказываются во много раз более стойкими даже при очень высоких нагревах при сравнении их с обычными стальными изделиями.
6. Практическое выполнение различных операций термической обработки. При выполнении на практике различных операций термической обработки необходимо знать: 1) химический состав и основные физико-химические свойства сталь; 2) цель термической обработки данного изделия; 3) величину, размеры и вес изделия.
Главнейшими физико-химическими свойствами, имеющими большое значение для термической обработки, являются: а) температуры превращений, испытываемых сталь данного химического состава, как при нагревании, так и при охлаждении; эти температуры обычно называют «критическими точками» стали, б) скорости отдельных процессов, из которых слагается превращение, испытываемое сталь при нагревании, а, следовательно, и при охлаждении.
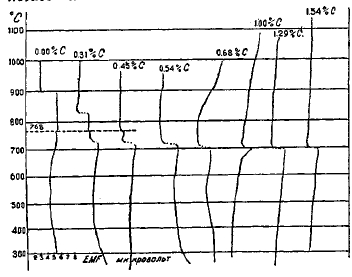
Фиг. 23. Кривые нагревания стали с различным содержанием углерода, записанные термоэлектрическим методом (J. Р. Т. Berliner).
Критические точки чистого железа были указаны выше; они обозначаются: при 769°—А2 (магнитное превращение), при 906°—A3 (превращение в гамма-железо и обратное), при 1400°—А4 (превращение в дельта-железо и обратное). Введение в сталь примесей, так или иначе реагирующих с железом, неизбежно отражается на положении критических точек; различие между отдельными примесями заключается лишь в том, что одни примеси изменяют положение критических точек сильно и заметно, другие — почти неуловимо для наших измерительных приборов; одни примеси повышают критические точки, другие, наоборот, вызывают понижение критических точек. Одной из наиболее сильнодействующих примесей сталь является углерод. Присутствие углерода оказывает заметное понижающее влияние на критические точки железа. Понижение критических точек наблюдается лишь до эвтектоидного содержания углерода — 0,80 - 0,85%, так как это содержание углерода соответствует предельной растворимости углерода в гамма-железе при температуре критической точки. Дальнейшее увеличение содержания углерода критической точки не изменяет, т. к. предел растворимости остается все тем же, и весь избыточный углерод присутствует в форме карбида железа (или же графита при известных условиях обработки). Общий характер влияния углерода на положение критических точек представлен на фиг. 23—25. На фиг. 25 также показана кривая SЕ предельной растворимости углерода в гамма-железе. Область между линиями GO и МО соответствует предполагаемой аллотропической форме бета железа, являющейся, по-видимому, лишь промежуточной формой при изменении кристаллической решетки гамма-железа в решетку альфа-железа.
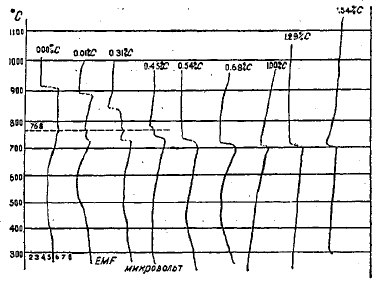
Фиг. 24. Кривые охлаждения тех же сортов стали, записанные тем же методом (J. F. T. Berliner).
Температура превращения эвтектоидной смеси S, соответствующая 700°—720°С, отмечается обязательно и при всех низших содержаниях углерода, так как это есть температура превращения перлита, смеси железа и карбида железа, имеющейся в сталь при всех содержаниях углерода. Температура эта носит название «критической точки А2».
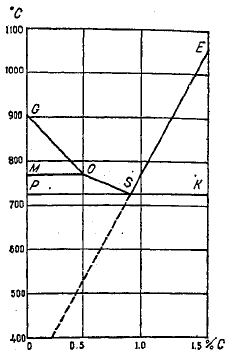
Фиг. 25. Влияние углерода на положение критических точек железа (Н. Scott).
Наиболее сильное влияние в сторону понижения критических точек оказывают на сталь две наиболее часто применяемые примеси: никель и марганец (фиг. 26 и 27). Кремний, алюминий и хром производят некоторое небольшое повышение критической точки А1, понижая в то же время точку А2; вольфрам повышает значительно точку A3; ванадий понижает А1, и повышает А2.
Влияние кобальта чрезвычайно характерно — кобальт повышает резко А1, в то же время А2 и А3 также сильно повышаются. Уран почти не оказывает влияния на критические точки стали.
Скорость отдельных процессов превращения, испытываемого сталью при охлаждении, играет первостепенную роль при установлении условий термической обработки. В зависимости от большей или меньшей скорости может быть получено, как указывалось уже выше, то или иное строение стали, те или иные свойства. Не остаются при этом без изменения также и критические точки стали. При постепенном увеличении скорости охлаждения наблюдаются следующие перемещения критической точки А2: 1) сначала температура превращения понижается лишь немного — в этом случае строение стали соответствует распавшемуся раствору с чрезвычайно мелким распределением частиц карбида; строение стали, видимое в микроскоп и окрашивающееся обычно при травлении шлифа соответствующими реактивами в темный цвет, носит название «тростит» (соответствует столбцу «мельчайшие частицы карбида и альфа-железо» в графике строения стали после охлаждения, диаграмма фиг. 22).
2) Затем, при дальнейшем увеличении скорости охлаждения вместо одной остановки A1 на кривых охлаждения начинают замечаться две остановки: одна, троститная, в области температур, сравнительно близких к нормальной температуре превращения, вторая — в области значительно более низких температур. Эта вторая остановка, обозначаемая в отличие от первой А”1 (первая остановка обозначается А'1), соответствует тем скоростям охлаждения, когда не успевает уже происходить полностью распадение твердого раствора, и часть атомов углерода остается растворенной в альфа-железе; остановка А”1 в этом случае соответствует процессу превращения гамма железа в альфа-железо, последующее же выделение атомов углерода не успевает произойти, вследствие значительного понижения теплового состояния металла при совершившемся превращении гамма — в альфа-железо. Сталь имеет строение резко различающееся: известная часть объема будет окрашенной в темный цвет и имеет все признаки строения тростита, другая же часть остается светлой, совершенно однородной, по строению имеющей ориентацию иголок, расположенных под различными углами. Такая структура носит название в металлографии «мартенсит».
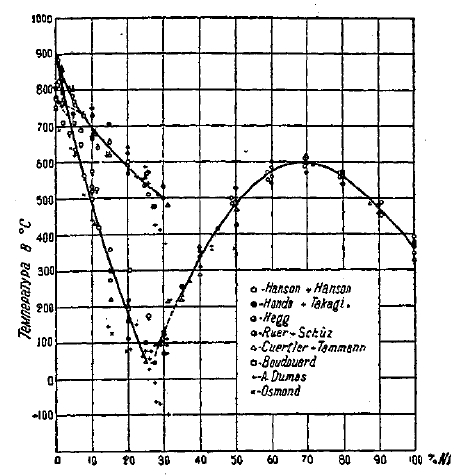
Фиг. 26. Влияние Ni на температуру магнитного превращения (А2 и А3) железа, по данным различных исследователей (Circular № 58 Bureau of Standards).
3) Увеличивая, далее скорость охлаждения, мы будем иметь возможность наблюдать постепенное уменьшение объемов тростита, постепенное распространение мартенситных областей, пока не получится более или менее сплошное строение полного мартенсита (отвечает ординате с на фиг. 22). Полученный при такой скорости охлаждения, называемой часто «критической скоростью», мартенсит отличается весьма большой однородностью, почти совершенным отсутствием иголок, столь типичных для структуры неполного мартенсита.
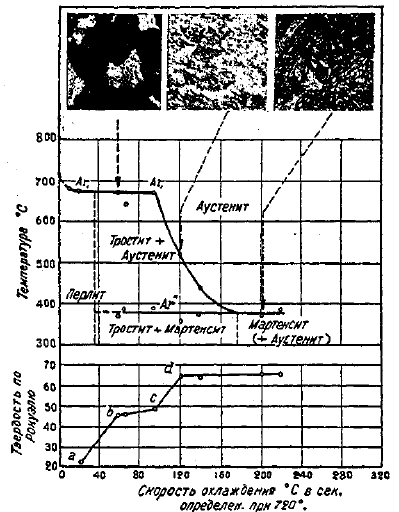
Фиг. 27. Влияние Mn на положение критических точек железа (H. Esser и P. Oberhoffer).
4) Далее, при возрастании скорости охлаждения, мы переходим в область совместного существования двух твердых растворов: а) углерода в альфа-железе (мартенсит) и б) углерода в гамма-железе, в последнем случае структура носит название «аустенит», при микроскопическом наблюдении аустенит имеет вид вполне однородного тела, сложенного из зерен, стремящихся иметь границы правильных многоугольников. При малом содержании аустенита в охлажденной стали его невозможно заметить и выделить при рассмотрении структуры в микроскоп, мартенсит же в этом случае становится снова игольчатым или даже крупно-игольчатым. Такое строение указывает на существование сильных внутренних напряжений в стали. Закономерность изменения критических точек стали при возрастании скорости охлаждения хорошо иллюстрируется диаграммой, экспериментально установленной Н. French и О. Klopsch в лаборатории Американского Бюро Стандартов (фиг. 28).
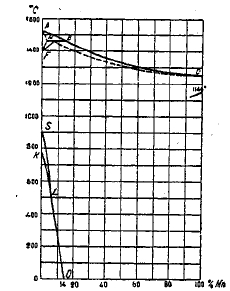
Фиг. 28. Диаграмма закалки стали, содержащей 0,75% углерода, охлаждавшейся с различной скоростью после нагрева до 800°C. Микроструктура (для ясности снимки авторов заменены снимками лаборатории завода «Красный Путиловец») получена при увеличении в 150 раз на поверхности образца, протравленного 4% раствором пикриновой кислоты а спирте.
Практически, при закалке небольших образцов скорость охлаждения в 175°—225° может быть получена при погружении нагретого куска стали в 5% раствор едкого натра в виде при температуре ванны в 20°. Скорость, охлаждения в различных жидкостях указана в таблице 4-ой составленной на основании данных Н. French и О. Klopsch.
Таблица 4.
Скорость (при 720°С) охлаждения в различных жидкостях стальных образцов, нагретых до высокой температуры.
|
Скорость охлаждения °С в секунду |
ЖИДКОСТЬ |
Температура ванны, °С |
|
175-225 |
5% раствор едкого натра в воде |
20 |
|
160-195 |
10% раствор поваренной соли в воде |
20 |
|
135-175 |
10-20% раствор серной кислоты в воде |
20 |
|
110-150 |
Вода |
20 |
|
85-135 |
Вода |
40 |
|
80-100 |
95% серной кислоты |
20 |
|
55-85 |
Вода |
60 |
|
25-80 |
Разные масла |
20 |
|
20-35 |
Вода |
80 |
|
10-15 |
Вода кипящая |
99,5 |
Третьим значительным фактором, определяющим условия термической обработки, являются размеры и объем обрабатываемого изделия, вернее говоря, отношение объема к поверхности. Чем больший объем будет приходиться на каждую единицу охлаждаемой поверхности изделия, тем меньшая скорость будет достигнута при охлаждении в совершенно идентичных условиях. Следовательно, при термической обработке массивных стальных изделий с высоким отношением объема к поверхности необходимо так видоизменять условия обработки, чтобы охлаждение шло приблизительно с той же скоростью, которая установлена для небольших тел. С другой стороны, при закалке больших и крупных изделий не достигается равномерность скорости охлаждения по всему сечению. Всегда охлаждение поверхности будет иметь скорость наибольшую, в то же время в центральных частях скорость охлаждения будет тем меньше, чем дальше отстоит рассматриваемый слой от поверхности. Практически этим обстоятельством пользуются при термической обработке инструментов, давая изделиям т. н. «внутренний отпуск», заключающийся в совершенном изъятии закаливаемого предмета из охлаждающей ванны в тот момент, когда его поверхность будет почти совсем холодной, внутри же температура еще достаточно высока. Теряя в дальнейшем при воздушном охлаждении лучеиспусканием запас аккумулированной внутри теплоты, переходящей благодаря теплопроводности в поверхностные закаленные слои металла, тем самым изделие самоотпускается, т. е. испытывает нагрев закаленных областей до таких приблизительно температур, до которых его пришлось бы нагревать особо после полного охлаждения всего объема в ванне.
Различные вводимые в сталь примеси оказывают заметное, иногда же чрезвычайно сильное замедляющее влияние на скорость процессов, совершающихся в стали и тем самым позволяют получать значительно большую «глубину закалки», чем это имеет место при закалке обыкновенной углеродистой стали.
Наиболее сильное замедление процессов вызывает в стали хром, называемый поэтому в английской литературе «ленивым» (sloggish) элементом. Также марганец, вольфрам, молибден, кобальт способны вызывать замедление процессов, в особенности же процесса распадения твердого раствора углерода в альфа-железе и образования карбида железа. Этим свойством специальной стали широко пользуется техника в области изготовления инструментальной стали для быстрого резания, так называемой «быстрорежущей стали», не теряющей своей твердости при разогреве до 500°; в области изготовления стали для горячей штамповки, горячего волочения и т. п.
Медь и никель также понижают скорости процессов, но уже менее значительно.
V. КОЛИЧЕСТВЕННАЯ ХАРАКТЕРИСТИКА ОСНОВНЫХ МЕХАНИЧЕСКИХ СВОЙСТВ СТАЛИ.
1. Упругость стали, являющаяся свойством кристаллической решетки сохранять свою форму и возвращать первоначальную форму после деформации, произведенной действием какой-либо внешней силы, при прекращении действия силы, количественно характеризуется величиной предела упругости, т. е. того напряжения, которое должно быть приложено к стали для преодоления упругих сил и получения остающейся деформации. Ввиду того, что сталь является телом, всегда обладающим известной большей или меньшей степенью неоднородности, как в смысле физического строения, так и в смысле распределения внутренних напряжений, то следовательно, и предельные напряжения упругого состояния, характеризующие упругие свойства решеток в различных бесконечно малых частях объема стали, также различаются по своей величине и иногда довольно значительно. Поэтому, при установлении предела упругости какого-либо сорта стали необходимо, применять метод статистический: определять предел упругости, присущий громадному большинству точек (бесконечно малых частей объема) изучаемого сорта стали. Получаемая величина, выраженная как напряжение в кг на кв. мм (в Англии и Америке в т на кв. дюйм, или в фунтах на кв. дюйм), может быть названа пределом упругости данного сорта стали при известной термической обработке его; эта величина называется часто также пределом текучести (Streckgrenze, Fliessgrenze, yield point, limite d’еcoulement limitе éiastiquе appаrente) стали.
С другой стороны, существующая степень неоднородности упругих сил в каждом отдельном испытываемом образце изучаемого сорта стали также может быть охарактеризована по тем первым незначительным пластическим деформациям, которые могут быть уловлены чувствительными приборами при испытании и которые соответствуют величине предела упругости в частях объема образца, наиболее ослабленных вследствие существования внутренних напряжений или присутствия посторонних включений.
Такую пониженную величину предела упругости определяют обычно условно, точно оговаривая в технических условиях, какая величина наблюдаемой деформации служит признаком достижения предела упругости, называемого в этом случае уже пределом пропорциональности. Более правильно характеризовать степень механической однородности испытываемого образца по отношению предела пропорциональности к пределу упругости материала (предел текучести); чем ниже будет это отношение, тем больше степень механической неоднородности материала.
Приписывание некоторыми русскими металлургами преимущественного и самодовлеющего значения пределу пропорциональности, как единственной и главной характеристике упругих свойств материала в целом, несомненно, является увлечением и заблуждением.
Упругие свойства стали характеризуются также и величиной упругой деформации, производимой напряжением одной и той же величины в образцах различных сортов стали или при различных условиях термической обработки образцов одной и той же стали. Упругая деформация стали определяется величиной коэффициента упругого удлинения. Если растягивающая сила Р вызывает упругое удлинение λ у образца длиной L с площадью поперечного сечения ω, то при напряжении σ=Р/ω получается относительная упругая деформация ε=λ/L, а коэффициент упругого удлинения α=ε/σ. Часто характеризуют упругую деформацию величиной М =1/α, называемой модулем упругости.
2. Прочность стали, определяемая величиной сил сцепления частиц металла, количественно характеризуется двумя величинами: 1) напряжением, отвечающим окончанию обшей пластической деформации образца при растяжении и началу образования интенсивного смешения частиц в некотором сечении образца (начало образования шейки) — это т. н. «временное сопротивление» (Zugfestigkeit, Іа charge de rupture, tensile strenght); 2) напряжением, испытываемым материалом в наиболее узкой части шейки в момент разрыва — «сопротивление при разрыве» (Bruchfestigkeit).
3. Пластические свойства стали, способность к деформации без разрушения при напряжениях, превышающих предел упругости, характеризуются обычно величиной относительного удлинения образца при растяжении. Эта величина удлинения складывается из двух отдельных деформаций: 1) общего увеличения длины образца по всему объему, происходящего до момента начала образования шейки, и 2) местного увеличения длины в месте, прилегающем к наиболее утончающемуся сечению образца (шейке), зависящего от величины самого сужения (диаметра образца в шейке). Благодаря суммированию двух различного рода деформаций, — одной пропорциональной длине образца, другой не зависящей от длины образца, — самая величина общего удлинения оказывается различной для образцов одинакового диаметра, но разной длины, приготовленных из одного и того же материала. Необходимо указывать поэтому каждый раз, к какой длине образца относится сообщаемая цифра удлинения.
4. Вязкость и физическая однородность строения стали проявляются при испытании на растяжение в форме определенной величины деформации в месте разрыва, в шейке. Чем больше сужение, чем однороднее материал, тем больше его вязкость. Те же свойства характеризуются и величиной удельной работы удара (resilience), определяемой по величине той работы, которую нужно затратить при ударе для разрушения образца в заранее намеченном (надрез) сечении определенной величины.
6. Твердость стали может быть определена: 1) методом вдавливания шарика (Бринель) с вычислением соответствующего числа твердости по различной деформации, производимой одной и той же силой; 2) методом вдавливания и вычисления силы, затрачиваемой на определенную деформацию (Мартенс); 3) видоизмененным методом Бринеля с применением весьма малых нагрузок и получением весьма малых деформаций (Роквел, Виккерс); 4) методом отскакивания бойка от поверхности испытываемого тела с измерением высоты, отскакивания (Шор, Совёр); 5) методом качания маятника, точка опоры которого поставлена на испытываемую поверхность: чем тверже тело, тем продолжительнее время 10 полных качаний маятника (Герберт). Менее совершенны способы определения твердости царапанием, к тому же самая идея метода царапания далека от физической природы свойства твердости, совершенно не связанного с явлением разъединения частиц. Сопротивление усталости стали характеризуется величиной тех напряжений, повторное, переменное или вибрационное приложение которых не вызывает преждевременного разрушения материала.
7. Сопротивление изнашиваемости сталь определяется различно в зависимости от применяемых приборов и в согласии с характером изнашивания работающих частей машин.
VI. ОПИСАНИЕ ГЛАВНЕЙШИХ СОРТОВ СТАЛИ И ИХ ТЕХНИЧЕСКОГО ПРИМЕНЕНИЯ.
1. Углеродистая сталь — см. табл. 5.
2. Кремнистая сталь — обладает после термической обработки высокими упругими свойствами, поэтому применялась долгое время как специальная рессорная сталь. Но недостаточная изотропность стали (различие свойств в разных направлениях) заставили заменить эту сталь другими сортами — кремне-марганцовистой, кремне-хромовой. Кроме того, при малом содержании углерода кремний повышает магнитную проницаемость стали и понижает потери на гистерезис, почему кремнистая сталь и применяется для изготовления листов трансформаторного и динамного железа. При содержании кремния выше 4% железо становится чрезвычайно хрупким. Типичные составы указаны в табл. 6-й.
3. Никелевая сталь. Применение никелевой стали чрезвычайно широко и разнообразно. Содержание углерода обычно не бывает выше 0,5%. Применение указано в табл. 7-й.
4. Медистая сталь — распространена сравнительно мало, но установленные многочисленными исследованиями последнего времени положительные качества медистой стали: повышение стойкости от окисления и ржавления железных листов с небольшим (0,3%) содержанием меди, повышение упругих свойств медистой стали после термической обработки — создают условия для расширения области применения медистой стали.
5. Марганцовистая и высокомарганцовистая сталь — распространена сравнительно широко. Высокомарганцовистая сталь, или сталь Гадфильда - непревзойденный никаким другим металлом материал по своему сопротивлению изнашиваемости и истираемости. Применение указано в табл. 8-й.
6. Хромовая и высокохромовая сталь — чрезвычайно сильно распространена, отличаясь своими превосходными качествами, сопротивлением изнашиванию, неокисляемостью (12% Сr). Применение указано в табл. 9.
7. Ванадиевая сталь – применяется редко как таковая. Гораздо чаще пользуются ванадием как дополнительной примесью к другим сортам специальной стали. Углеродистая ванадиевая сталь применяется для изготовления стальных отливок повышенной прочности (0,25-0,35% С; 0,15-0,25% V); для получения чистой и не хрупкой инструментальной стали (1,0-1,2% С; 0,5-0,8% V).
8. Вольфрамовая сталь — используется практикой с самым разнообразным содержанием вольфрама, от 0,5% до 9%, главнейшим образом в области изготовления инструментальной стали и сталь для постоянных магнитов.
9. Молибденовая сталь — самостоятельного значения не имеет, так как молибден вводится исключительно как дополнительная примесь в различные сорта специальной стали.
10. Кобальтовая сталь — кобальт обычно используется для изготовления стали с прибавлением добавочных элементов (хром, вольфрам), такая сложная сталь имеет громадное значение в области приготовления постоянных магнитов.
11. Машиноподелочная сталь сложного состава; сюда относится хромоникелевая, хромованадиевая, хромомарганцовистая, хромо-никель-вольфрамовая, хромоникельмолибденовая сталь Характеристика состава и главнейших свойств приведена в табл. 10-й.
12. Инструментальная сталь сложного состава: хромовольфрамовая, хромо-вольфрамо-ванадиевая, хромо-вольфрамо-кобальтовая, хромо-вольфрамо-молибденовая. Характеристика состава показана в табл. 11.
13. Сталь и стальные сплавы особого назначения. Сюда относятся: 1) группа сплавов железа и никеля с различного рода особенностями в тепловом расширении; инвар (36% Nі), коэффициент расширения близок к нулю первое время после изготовления; платинит — коэффициент расширения платины и стекла, фиксинвар — разновидность инвара с низким и устойчивым во времени коэффициентом теплового расширения; элинвар — сплав железа, никеля и хрома, обладающий весьма устойчивым при колебаниях температуры модулем упругости; 2) группа сплавов железа и хрома (до 24%), обладающих стойкостью против разъедающего действия кислот; 3) сплавы железа с кобальтом и небольшим количеством марганца, хрома или вольфрама — с чрезвычайно сильным развитием магнитной задерживательной силы (сплав К. S.); 4) сплавы железа с никелем и хромом или с никелем и марганцем — являющиеся совершенно немагнитным металлом; 5) сплавы железа с кремнием — хрупкие, но трудно разъедаемые кислотами.
В табл. 12-й приведены данные, характеризующие более подробно свойства некоторых распространенных сортов стали и стальных сплавов.
Н. Гудцов.
Таблица 5
Применение различных сортов углеродистой стали (по P. Oberhoffer с изменениями)
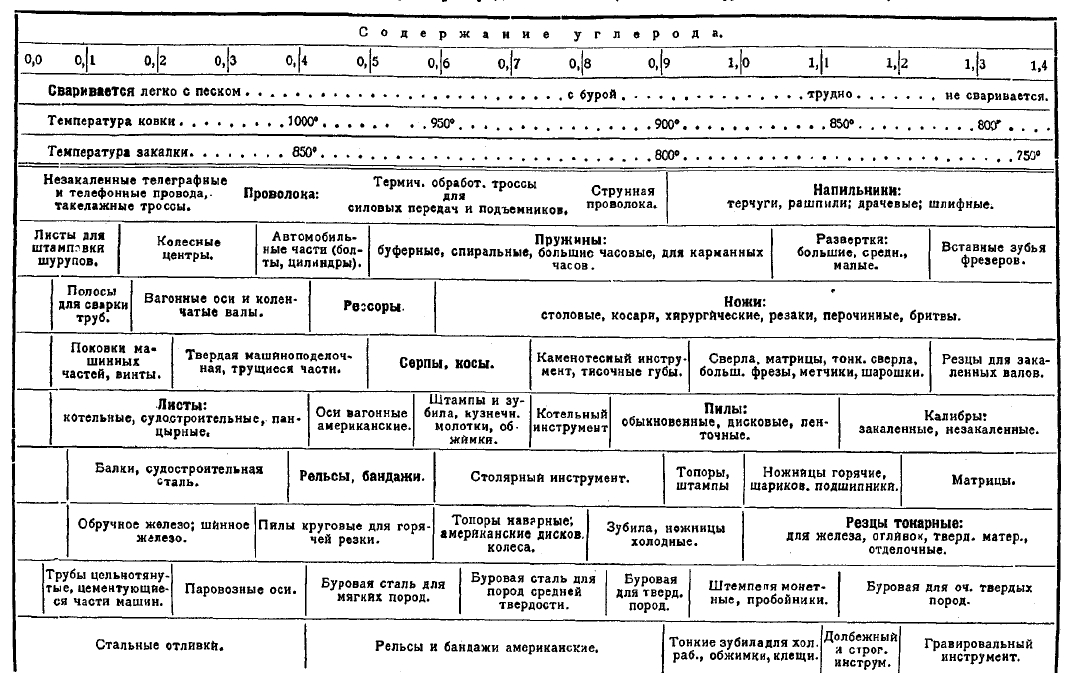
Таблица 6.
Применение кремнистой стали (по G. Mars и др. источники).
|
Назначение стали |
Химический состав в % |
||
|
C |
Si |
Mn |
|
|
Листы динамные |
0,0-0,1 |
0,7-1,0 |
0,3 |
|
- |
- |
2,0-4,0 |
0,0-0,1 |
|
Рессорная сталь средней твердости |
0,45-0,55 |
1,0-1,5 |
0,4-0,5 |
|
То же, твердая |
0,3-0,5 |
2,5 |
- |
|
Листы трансформаторные |
0,0-0,1 |
1,0-2,0 |
0,1-0,3 |
|
Зубила |
0,3-0,4 |
Около 2 |
- |
|
Диафрагмы телефонные |
- |
3,0-4,0 |
- |
Таблица 7
Применение никелевой стали
|
Назначение стали по различным спецификациям |
Химический состав в % |
||||
|
C |
Mn |
P |
S |
Ni |
|
|
I. По германским источникам: |
|
|
|
|
|
|
Заклепки, листы, трубы |
0,05-0,15 |
- |
- |
- |
1-2 |
|
Листы котельные, сталь мостовая и пушечная |
0,2-0,45 |
- |
- |
- |
1,5-3,5 |
|
Части машин и автомобилей цементующиеся (болты, валики распределительные, колеса зубчатые и цепные, кулаки, цапфы и т. п.) |
0,05-0,15 |
- |
- |
- |
2,5-8 |
|
Валы коленчатые и трансмиссии, оси, шатуны |
0,2-0,45 |
- |
- |
- |
3-5 |
|
Болты, колеса зубчатые, цапфы – без цементации |
0,25-0,45 |
- |
- |
- |
4-6 |
|
II. Спецификация Am. S. T. M.: |
|
|
|
|
|
|
Сталь заклепочная |
<0.3 |
<0.6 |
<0.04 |
<0.045 |
>3.25 |
|
Сталь строительная |
<0.45 |
<0.7 |
<0.05 |
<0.05 |
>3.25 |
|
III. Спецификация S. A. E.: |
|
|
|
|
|
|
Автомобильная сталь, валики распределительные и т. п. |
0,1-0,2 |
0,3-0,6 |
max 0,04 |
max 0,045 |
3,25-3,75 |
|
Крестовины, шестерни |
0,15-0,25 |
0,5-0,8 |
max 0,04 |
max 0,045 |
3,25-3,75 |
|
Кулаки, оси передние |
0,25-0,35 |
0,5-0,8 |
max 0,04 |
max 0,045 |
3,25-3,75 |
|
Валы коленчатые и т. п. |
0,3-0,4 |
0,5-0,8 |
max 0,04 |
max 0,045 |
3,25-3,75 |
|
Шестерни кор. спор. |
0,35-0,45 |
0,5-0,8 |
0,04 |
0,045 |
3,25-3,75 |
|
Валики, тяги и т. п. |
0,4-0,5 |
0,5-0,8 |
0,04 |
0,045 |
3,25-3,75 |
|
Звездочки цепные и т. п. |
0,45-0,55 |
0,5-0,8 |
0,04 |
0,045 |
3,25-3,75 |
|
Пальцы поршней и т. п. |
Не более 0,17 |
0,3-0,6 |
0,04 |
0,045 |
4,5-5,25 |
|
IV. Спецификация J. A. S. B.: |
|
|
|
|
|
|
Авиационная сталь |
0,1-0,2 0,15-0,25 0,2-0,3 |
0,3-0,6 0,3-0,6 0,5-0,8 |
0,04 0,04 0,04 |
0,045 0,045 0,045 |
3,25-3,75 3,25-3,75 3,25-3,75 |
|
V. Железо-никелевые сплавы: |
|
|
|
|
|
|
Клапана двигателей внутреннего сгорания, компасные коробки (немагнитная сталь), проволока высокого электрического сопротивления |
0,3-0,5 |
- |
- |
- |
25-28 |
|
Сплав «Инвар» с низким коэффициентом расширения |
0,5 |
0,5 |
- |
- |
35-38 |
|
Сплав «Платинит» с коэффициентом расширения платины и стекла |
0,15 |
- |
- |
- |
46 |
|
Сплав «Периалой» с весьма высокой магнитной проницаемостью |
0,04 |
- |
- |
- |
88,5 |
Таблица 8
Применение марганцовистой стали (по G. Mars и др. источники).
|
Назначение стали |
Химический состав, % |
||
|
C |
Mn |
Si |
|
|
Штампы и матрицы для горячей работы, наковальни |
0,4-0,5 |
0,8-1,2 |
- |
|
Пружины (в США) |
0,6-0,7 |
1,0-1,2 |
- |
|
Метчики, развертки, сверла для расп. болт. |
0,8-1,0 |
1,0-1,5 |
- |
|
Оправки, бородки |
0,45-0,5 |
1,2-1,4 |
0,1-0,2 |
|
Резервуары, баллоны для углекислоты |
0,25-0,35 |
1,3-1,4 |
0,1-0,2 |
|
Бандажи специальные |
0,3-0,4 |
1,3-1,4 |
0,1-0,2 |
|
Рессоры, оправки для прокатки труб |
0,4-0,5 |
1,6-2,0 |
- |
|
Доски волочильные |
1,6-1,8 |
1,6-2,0 |
0,1-0,2 |
|
Болты, козырьки и другие части землечерпалок, доски дробильные, заклепки специальные, крестовины, рельсы и пр. (С. Гадфильда) |
0,9-1,3 |
10-15 |
0,2-0,4 |
|
Сталь немагнитная для компасов и авиационных листов |
1,0-1,3 |
12-15 |
0,3-0,4 |
Таблица 9
Применение различных сортов хромовой стали (по G. Mars, P. Oberhoffer и другие источники).
|
Назначение стали |
Химический состав % |
|||
|
C |
Mn |
Si |
Cr |
|
|
Ролики с цементацией (США) |
0,15-0,20 |
- |
- |
0,4-0,6 |
|
Шламы |
0,3-0,35 |
0,7-0,8 |
0,8-0,9 |
0,4-0,6 |
|
Полотна пил, резцы прорезные, сверла спиральные |
0,9-1,0 |
0,1-0,3 |
0,1-0,3 |
0,4-0,6 |
|
Инструмент отдел., напильники для точки пил, ножи для бритв и для кожи, резцы токарные и строгальные, фрезы |
1,3-1,5 |
0,1-0,2 |
0,1-0,3 |
0,3-0,7 |
|
Зубила ручные |
0,6-0,7 |
- |
- |
0,6-0,9 |
|
Ножи для ножниц, штампы для горячей штамповки |
0,8-1,0 |
- |
- |
0,5-1,0 |
|
Спецификация A.S.T.M. на автомобильную сталь |
0,15-0,25 |
0,3-0,6 |
- |
0,6-0,9 |
|
0,35-0,45 |
0,5-0,8 |
- |
0,8-1,1 |
|
|
0,45-0,55 |
0,5-0,8 |
- |
0,8-1,1 |
|
|
0,95-1,1 |
0,2-0,5 |
- |
1,2-1,5 |
|
|
Листы для штамповки частей |
0,35-0,45 |
0,5-0,6 |
0,2-0,3 |
0,9-1,1 |
|
Пружины, рессоры |
0,40-0,50 |
0,7-0,9 |
0,15-0,25 |
0,9-1,1 |
|
Шарики для подшипников |
0,85-1,05 |
0,15-0,25 |
0,20-0,30 |
1,0-1,3 |
|
Зубила пневматические |
0,3-0,5 |
0,10-0,30 |
0,1-0,3 |
1,0-1,5 |
|
Кулачки, обоймы подшипника |
0,9-1,1 |
0,10-0,30 |
0,2-0,3 |
1,0-1,6 |
|
Обоймы для роликовых подшипников с цементацией (США) |
0,15-0,25 |
- |
- |
1-2 |
|
Рессоры вагонные |
0,2-0,4 |
0,2-0,4 |
0,1-0,3 |
1,3-1,7 |
|
Магниты постоянные |
0,8-0,9 |
0,3-0,5 |
- |
2,3-2,9 |
|
Диски волочильные (1) |
1,5-1,8 |
0,2-0,3 |
0,2-0,4 |
2,0-2,5 |
|
Диски волочильные (2) |
1,6-2,0 |
0,3-0,4 |
0,2-0,4 |
5-7 |
|
Диски волочильные (3) |
1,8-2,2 |
0,3-0,4 |
0,2-0,4 |
9-11 |
|
Валки для холодной прокатки, пробойники, штемпели |
0,8-1,0 |
0,2-0,3 |
0,2-0,3 |
2-4 |
|
Валки для калибровки, ножницы для резки горячего металла |
1,0-1,4 |
- |
- |
3-5 |
|
Клапана двигателей внутреннего сгорания |
0,3-0,4 |
0,4-0,5 |
0,4-0,5 |
11-14 |
|
Нержавеющее железо |
0,05-0,2 |
- |
- |
11-15 |
|
Нержавеющая сталь |
0,2-0,6 |
- |
- |
12-16 |
Таблица 10
Химический состав машиноподелочной стали с двумя и более примесями
|
Назначение стали по различным спецификациям |
Химический состав стали в % |
|||||||
|
C |
Mn |
Si |
S не более |
Р не более |
Ni |
Cr |
|
|
|
I. Кремнемарганцовистая сталь |
|
|
|
|
|
|
|
|
|
Спецификация S.A.E. |
|
|
|
|
|
|
|
|
|
Автомобильная рессорная |
0,45-0,55 |
0,6-0,9 |
1,8-2,2 |
0,045 |
0,045 |
- |
- |
- |
|
0,55-0,65 |
0,6-0,9 |
1,8-2,2 |
0,045 |
0,045 |
- |
- |
- |
|
|
0,55-0,65 |
1,5-1,8 |
1,5-1,8 |
0,045 |
0,045 |
- |
- |
- |
|
|
II. Хромоникелевая сталь |
|
|
|
|
|
|
|
|
|
Спецификация S.A.E. |
0,1-0,2 |
0,3-0,6 |
|
0,04 |
0,04 |
1-1,5 |
0,45-0,75 |
- |
|
Автомобильная с 1,25% Ni |
0,15-0,25 |
0,3-0,6 |
|
0,045 |
0,04 |
1-1,5 |
0,45-0,75 |
- |
|
0,2-0,3 |
0,5-0,8 |
|
0,045 |
0,04 |
1-1,5 |
0,45-0,75 |
- |
|
|
0,25-0,35 |
0,5-0,8 |
|
0,045 |
0,04 |
1-1,5 |
0,45-0,75 |
- |
|
|
0,3-0,4 |
0,5-0,8 |
|
0,045 |
0,04 |
1-1,5 |
0,45-0,75 |
- |
|
|
0,35-0,45 |
0,5-0,8 |
|
0,045 |
0,04 |
1-1,5 |
0,45-0,75 |
- |
|
|
Автомобильная с 1,75% Ni |
0,1-0,2 |
0,3-0,6 |
|
0,04 |
0,04 |
1,5-2 |
0,9-1,25 |
|
|
0,15-0,25 |
0,3-0,6 |
|
0,04 |
0,04 |
1,5-2 |
0,9-1,25 |
|
|
|
0,25-0,35 |
0,3-0,6 |
|
0,04 |
0,04 |
1,5-2 |
0,9-1,25 |
|
|
|
0,35-0,45 |
0,3-0,6 |
|
0,04 |
0,04 |
1,5-2 |
0,9-1,25 |
|
|
|
0,4-0,5 |
0,3-0,6 |
|
0,04 |
0,04 |
1,5-2 |
0,9-1,25 |
|
|
|
0,45-0,55 |
0,3-0,6 |
|
0,04 |
0,04 |
1,5-2 |
0,9-1,25 |
|
|
|
Автомобильная с 3% Ni |
0,1-0,2 |
0,45-0,75 |
|
0,04 |
0,04 |
2,75-3,25 |
0,6-0,95 |
|
|
0,3-0,4 |
0,45-0,75 |
|
0,04 |
0,04 |
2,75-3,25 |
0,6-0,95 |
|
|
|
0,45-0,55 |
0,45-0,75 |
|
0,04 |
0,04 |
2,75-3,25 |
0,6-0,95 |
|
|
|
Автомобильная с 3,5% Ni |
|
|
|
0,04 |
0,04 |
3,25-3,75 |
1,25-1,75 |
- |
|
|
|
|
0,04 |
0,04 |
3,25-3,75 |
1,25-1,7 |
- |
|
|
|
|
|
0,04 |
0,04 |
3,25-3,75 |
1,25-1,75 |
- |
|
|
|
|
|
0,04 |
0,04 |
3,25-3,75 |
1,25-1,75 |
- |
|
|
Спецификация французского воздухоплавательного ведомства (Grard): |
|
|
|
|
|
|
|
|
|
Сталь цементитная для частей, испытывающая высокое напряжение и удары (валик поршня, шестерни …) |
|
|
|
0,04 |
0,04 |
2,25-2,75 |
0,45-0,75 |
- |
|
Сталь шестеренная |
|
|
|
0,04 |
0,04 |
2,35-2,85 |
0,55-0,85 |
- |
|
Сталь полутвердая, для частей, подвергшихся усталости (валы коленчатые и проп., клапана впуска, шатун) |
0,28-0,35 |
0,25-0,55 |
0,2-0,3 |
0,04 |
0,04 |
2,5-2,8 |
0,55-0,85 |
|
|
Сталь твердая для тех же частей |
0,3-0,35 |
0,1-0,4 |
0,2-0,4 |
0,04 |
0,04 |
3,0-3,5 |
1,0-1,5 |
|
|
Сталь самозакаливающаяся (клапана, ролики, шатун, шестерни) |
0,25-0,4 |
0,4-0,6 |
0,2-0,3 |
0,04 |
0,04 |
3,5-5 |
1,2-2 |
|
|
Спецификация германская (P. Oberhoffer) |
|
|
|
|
|
|
|
|
|
Сталь артиллерийская |
0,38-0,42 |
0,5-0,6 |
0,3-0,4 |
|
|
1,8-2 |
0,75-1 |
|
|
Сталь для высоконапряженных автомобильных и машинных частей |
0,25-0,45 |
|
|
|
|
2,5-2,75 |
0,25-1 |
|
|
Сталь цементирующаяся (1) |
0,05-0,15 |
0,35-0,5 |
0,2-0,3 |
|
|
2,5-2,8 |
0,5-0,8 |
|
|
Сталь цементирующаяся (2) |
0,05-0,15 |
0,35-0,5 |
0,2-0,3 |
|
|
3,5-4,5 |
1,4-1,7 |
|
|
Сталь цементирующаяся (3) |
0,2-0,22 |
0,35-0,5 |
0,2-0,3 |
|
|
3,55-4,0 |
1,4-1,7 |
|
|
Сталь для коленчатых валов (1) |
0,35-0,5 |
0,35-0,5 |
0,2-0,3 |
|
|
2,5-3,5 |
1,3-1,5 |
|
|
Сталь для коленчатых валов (2) |
0,35-0,5 |
0,35-0,5 |
0,2-0,3 |
|
|
4,0-4,5 |
1,3-1,5 |
|
|
Хромоникелевая сталь завода Фирт. |
0,28-0,34 |
0,45-0,7 |
Max 0,3 |
|
|
3,0-3,75 |
0,5-1 |
|
|
|
0,25-0,32 |
0,35-0,6 |
Max 0,3 |
|
|
4,0-4,5 |
1,0-1,5 |
|
|
Хромоникелевая сталь завода Виккерс: Мягкая |
0,18-0,25 |
0,25-0,55 |
Max 0,3 |
|
|
3,25-4 |
0,4-0,8 |
|
|
Средней твердости |
0,25-0,35 |
0,25-0,55 |
Max 0,3 |
|
|
3,25-4 |
0,45-0,75 |
|
|
Твердая |
0,3-0,4 |
0,25-0,6 |
Max 0,3 |
|
|
3,25-4 |
0,45-0,75 |
|
|
Самозакаливающаяся |
0,25-0,35 |
0,35-0,55 |
Max 0,3 |
|
|
3,5-4,25 |
1,0-1,5 |
|
|
Хромоникелевая завода «Красный Путиловец» (1) |
0,2-0,3 |
0,3-0,6 |
Max 0,3 |
0,04 |
0,04 |
2,5-3 |
0,9-1,25 |
|
|
Хромоникелевая завода «Красный Путиловец» (2) |
0,1-0,2 |
0,3-0,6 |
Max 0,3 |
0,04 |
0,04 |
3,5-4 |
0,9-1,25 |
|
|
Хромоникелевая завода «Красный Путиловец» (3) |
0,1-0,2 |
0,3-0,6 |
Max 0,3 |
0,04 |
0,04 |
1,5-2 |
0,6-0,9 |
|
|
Хромоникелевая завода «Красный Путиловец» (4) |
0,2-0,3 |
0,3-0,6 |
Max 0,3 |
0,04 |
0,04 |
1,25-1,75 |
0,5-0,8 |
|
|
Хромоникелевая завода «Красный Путиловец» (5) |
0,1-0,2 |
0,3-0,6 |
Max 0,3 |
0,045 |
0,04 |
1,5-2 |
0,55-0,85 |
|
|
Хромоникелевая завода «Красный Путиловец» (6) |
0,3-0,4 |
0,5-0,8 |
Max 0,3 |
0,045 |
0,04 |
3,25-3,75 |
0,45-0,75 |
|
|
III. Хромо-никель-молибденовая сталь |
|
|
|
|
|
|
|
Мо |
|
Одного из заводов США |
0,25-0,35 |
0,5-0,8 |
|
|
|
2,75-3,25 |
0,7-1 |
0,3-0,5 |
|
По Greaves и Jones |
0,2-0,4 |
0,2-0,9 |
0,1-0,2 |
|
|
1,7-3,7 |
0,6-1,2 |
0,3-1,1 |
|
По Gillet и Mack |
0,2-0,6 |
0,4-0,6 |
0,1-0,2 |
0,04 |
0,04 |
1,0-3,2 |
0,4-1,5 |
0,2-1,5 |
|
IV. Хромо-никель-вольфрамовая сталь |
|
|
|
|
|
|
|
W |
|
По Gocrens |
0,3-0,4 |
|
|
|
|
3,75-4,25 |
1,25-1,75 |
0,8-1,2 |
|
По Grard |
0,2-0,3 |
0,2-0,4 |
0,2-0,4 |
0,04 |
0,04 |
4,25-4,75 |
0,2-0,4 |
2,15-2,65 |
|
V. Высокохромоникелевая сталь |
|
|
|
|
|
|
|
|
|
Сталь для труб лопаток (германская) |
0,2-0,4 |
|
|
|
|
2-4 |
10-14 |
|
|
По Gocrens |
0,1-0,2 |
|
|
|
|
0,5-1,5 |
14-16 |
|
|
VI. Кремнехромовая сталь |
|
|
|
|
|
|
|
|
|
Сталь для пружин, клапанов и прочих мелких, для рессор |
0,5-0,6 |
0,3-0,4 |
0,95-1,15 |
|
|
|
0,6-0,8 |
|
|
VII. Хромомарганцовистая сталь |
|
|
|
|
|
|
|
|
|
По Kolhiny |
0,2-0,4 |
0,7-0,9 |
|
|
|
|
1,1-1,5 |
|
|
Завода Ford |
0,4-0,5 |
0,7-0,9 |
|
|
|
|
0,9-1,1 |
|
|
Завода «Красный Путиловец» |
0,3-0,4 |
0,8-1,0 |
|
|
|
|
1,0-1,2 |
|
|
VIII. Хромованадиевая сталь |
|
|
|
|
|
|
|
|
|
Спецификация германских заводов (по Р. Oberhoffer): |
|
|
|
|
|
|
|
V не менее |
|
1) Цементирующаяся |
0,12-0,15 |
0,1-0,3 |
|
|
|
0,2-0,4 |
|
0,12 |
|
2) Сталь, применяемая в отожженном состоянии – для осей ведущих и легких, тяг и штоков, и в термически обработанном состоянии – для коленчатых валов, зубчатых колес и частей передачи |
0,25-0,3 |
0,4-0,5 |
|
|
|
1,1-1,9 |
|
0,16-0,18 |
|
3) Сталь, применяемая в отожженном состоянии – для колес железных дорог, пальцев кривошипа, и в термически обработанном состоянии – для рессор автомобилей, вагонных и паровозных. |
0,45-0,55 |
0,8-1,0 |
|
|
|
1,1-1,4 |
|
0,18 |
|
Спецификация S.A.E. и A.S.T.M. |
|
|
|
|
|
|
|
|
|
Сталь автомобильная |
0,15-0,25 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
0,2-0,3 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
|
0,25-0,35 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
|
0,3-0,4 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
|
0,35-0,45 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
|
0,4-0,5 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
|
0,45-0,55 |
0,5-0,8 |
|
0,04 |
0,04 |
|
0,8-1,1 |
0,15 |
|
|
0,9-1,05 |
0,2-0,45 |
|
0,03 |
0,03 |
|
0,8-1,1 |
0,15 |
|
|
Сталь рессорная |
0,55-0,65 |
0,6-0,9 |
|
0,05 |
0,04 |
|
0,8-1,1 |
0,15 |
|
Завода Фирт (Judge) |
0,37-0,42 |
0,6-0,85 |
|
|
|
|
1,2-1,4 |
0,16-0,2 |
|
Сталь для обойм шарикоподшипников и роликов (Grard) |
0,9-1,1 |
0,2-0,4 |
|
0,04 |
0,04 |
|
1,4-1,6 |
0,2-0,3 |
Таблица 11
Химический состав инструментальной специальной стали с двумя и более примесями
|
Назначение стали по различным спецификациям |
Химический состав % |
|||||||
|
C |
Mn |
Si |
Cr |
W |
V |
Mo |
|
|
|
I. Американская быстрорежущая сталь (по H. French и J. Strauss): |
|
|
|
|
|
|
|
|
|
1) Маловольфрамовая – высокованадиевая |
0,56-0,74 |
0,1-0,4 |
0,1-0,5 |
2,2-4,4 |
11-14 |
0,5-2,2 |
- |
|
|
2) Средневольфрамовая |
0,62-0,71 |
0,1-0,4 |
0,1-0,5 |
3-4,7 |
14-16 |
0,7-2,1 |
- |
|
|
3) Высоковольфрамовая - малованадиевая |
0,55-0,85 |
0,1-0,4 |
0,1-0,5 |
2,3-4,7 |
16-20 |
0,5-1,2 |
- |
Со |
|
4) Кобальтовая |
0,58-0,88 |
0,1-0,4 |
0,1-0,4 |
2,8-4,3 |
13-19 |
0,9-1,6 |
- |
1,9-4,7 |
|
5) Молибденовая |
0,6-0,69 |
0,1-0,4 |
0,1-0,5 |
3,5-4 |
13-17 |
1,1-2 |
0,5-0,7 |
- |
|
6) Кобальтмолибденовая |
0,65 |
0,1-0,4 |
0,1-0,5 |
4,25 |
18 |
1 |
1,1 |
4,9 |
|
7) Урановая |
0,58-0,8 |
0,1-0,4 |
0,1-0,5 |
3,2-3,9 |
14-20 |
0,8-1,4 |
- |
U: 0,19-0,26 |
|
II. Американская инструментальная по A.S.S.T. Handbook: |
|
|
|
|
|
|
|
|
|
1) Хромовольфрамовая: |
|
|
|
|
|
|
|
|
|
Метчики |
1,0-1,2 |
- |
- |
0,5-1 |
1-2 |
- |
- |
|
|
Отделочные инструменты |
1,1-1,3 |
- |
- |
1,-1,5 |
4,5-6 |
- |
- |
|
|
Недеформирующиеся |
1 |
1-1,25 |
- |
0,5 |
0,5 |
- |
- |
|
|
2) Хромо-вольфрамо-ванадиевая: |
|
|
|
|
|
|
|
|
|
Для штамп. гор. |
0,3-0,45 |
- |
- |
2,5-3,5 |
8-11 |
0,3-0,6 |
- |
|
|
Для пробойников |
0,3-0,55 |
- |
- |
1,25-2 |
1,5-2,5 |
0,15-0,4 |
- |
|
|
Для отдельных инструментов |
1,35-1,5 |
- |
- |
0,5-1 |
3,5-5 |
0,2-0,3 |
- |
|
|
III. Английская быстрорежущая по T. H. Nelson: |
|
|
|
|
|
|
|
|
|
Маловольфрамовая |
0,5-0,7 |
Max 0,2 |
Сл. |
2,5-3 |
12-14 |
Сл. |
- |
|
|
Средневольфрамовая |
0,55-0,65 |
Max 0,2 |
Сл. |
2,75-3,5 |
14-16 |
До 0,05 |
- |
|
|
Высоковольфрамовая |
0,55-0,65 |
Max 0,2 |
Сл. |
3-4 |
16-18 |
0,5-1 |
- |
|
|
IV. Германская инструментальная по P. Oberhoffer: |
|
|
|
|
|
|
|
|
|
Хромомолибденовая |
1-1,2 |
Max 0,35 |
Max 0,25 |
1-1,2 |
- |
- |
0,5-0,7 |
|
|
Быстрорежущая |
0,5-0,6 |
Max 0,35 |
Max 0,25 |
4-4,5 |
13-14 |
- |
- |
|
|
0,5-0,6 |
Max 0,35 |
Max 0,25 |
4-4,5 |
13-14 |
0,3-0,5 |
- |
|
|
|
0,55-0,65 |
Max 0,35 |
Max 0,25 |
4-5 |
18-20 |
- |
- |
|
|
|
0,55-0,65 |
Max 0,35 |
Max 0,25 |
4-5 |
18-20 |
0,3-0,5 |
- |
|
|
|
0,6-0,7 |
Max 0,35 |
Max 0,1 |
4-5 |
22-25 |
1 |
- |
|
|
|
0,6-0,65 |
Max 0,35 |
Max 0,35 |
4,2-4,6 |
9-9,5 |
0,2-0,5 |
3,5-4 |
Со |
|
|
0,6-0,7 |
Max 0,35 |
Max 0,35 |
4-5 |
12-13 |
0,3-0,5 |
3,5-4 |
1,5 |
|
|
1,5-1,6 |
Max 0,45 |
0,3-0,4 |
11-12 |
- |
- |
0,4-0,5 |
3,5 |
|
|
V. Русская инструментальная сталь («Красный Путиловец»): |
|
|
|
|
|
|
|
|
|
Хромовольфрамовая |
0,7-0,9 |
0,1-0,3 |
0,1-0,3 |
0,3-0,5 |
1-1,2 |
- |
- |
|
|
|
1-1,2 |
0,1-0,3 |
0,1-0,3 |
0,8-1 |
4-6 |
- |
- |
|
|
Быстрорежущая |
0,55-0,65 |
0,1-0,3 |
0,1-0,3 |
3,5-4,5 |
16-18 |
- |
- |
|
|
|
0,55-0,65 |
0,1-0,3 |
0,1-0,3 |
3,5-4,5 |
18-20 |
0,8-1 |
- |
|
Таблица 12
Механические свойства некоторых сортов стали и стальных сплавов (по «Circular of the Burean of Standards», № 101).
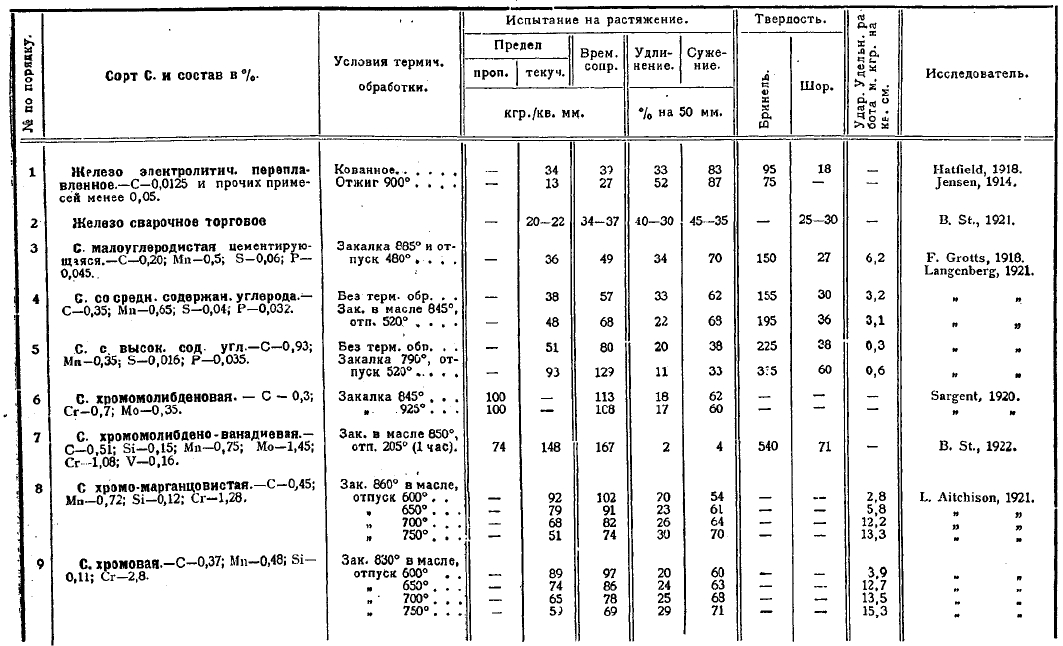
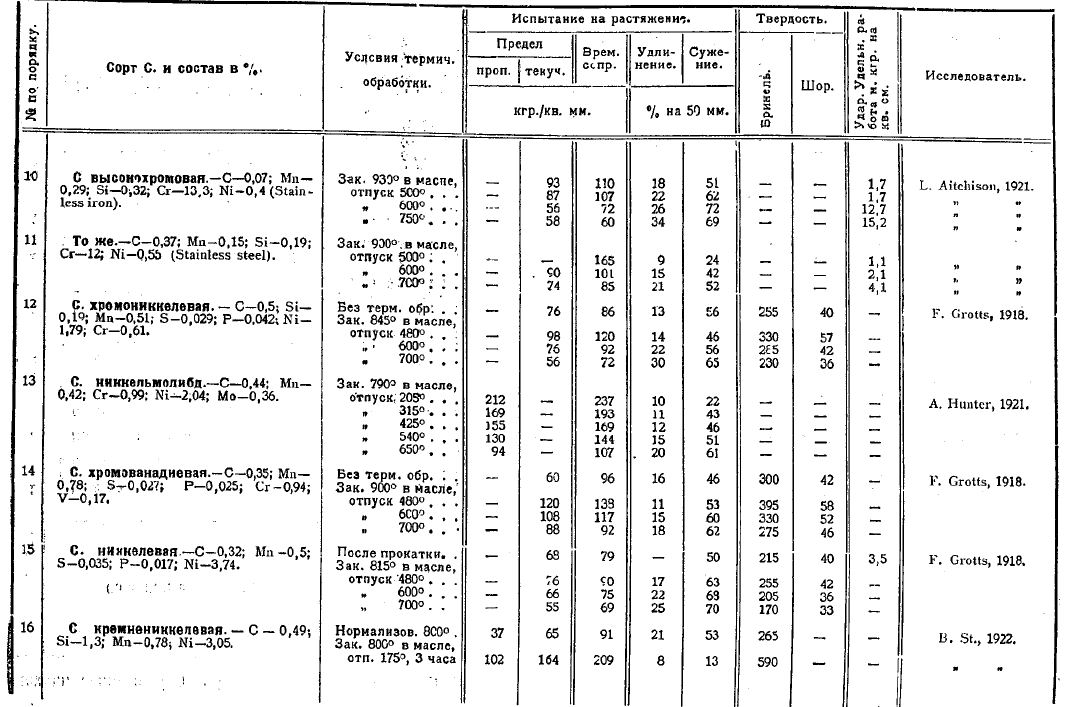
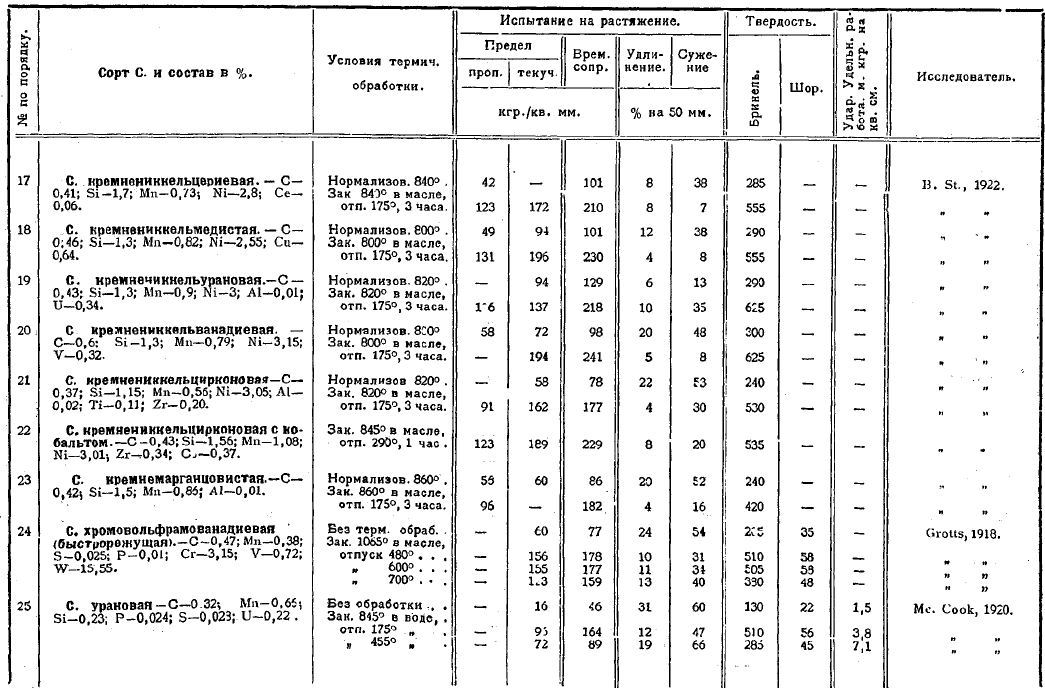
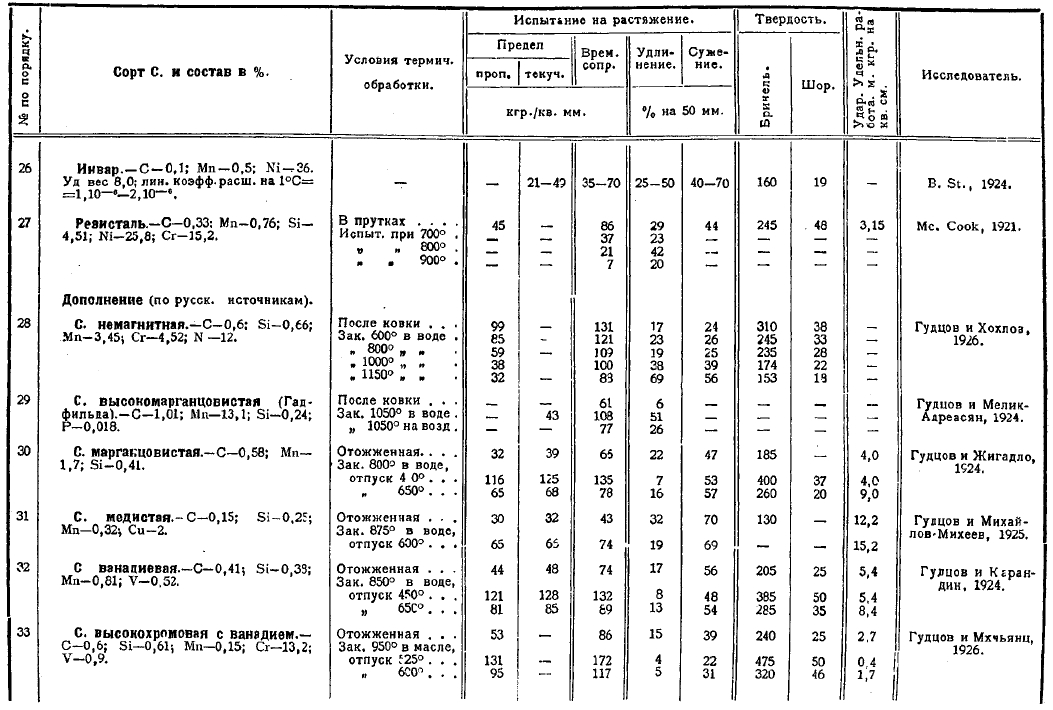
| Номер тома | 41 (часть 4) |
| Номер (-а) страницы | 321 |
