Терпены
Терпены, углеводороды (см.) ряда СnН2n-4, формулы С10Н16, широко распространены в растительном царстве, где они входят в состав эфирных масел, а также составляют главную массу живицы (см.), или терпентина хвойных пород, то есть жидкости, вытекающей из надрезов коры хвойных деревьев. Скипидар (см.), получающийся при перегонке терпентина или частей хвойных деревьев, состоит почти исключительно из терпенов. Как в виде эфирных масел, широко применяемых в парфюмерии, так и в виде скипидара и продуктов, добываемых из последнего, терпены широко применяются в технике и медицине. Связанные с терпенами кислородные соединения, к которым относится общеизвестная камфара, С10Н16О, сопровождают терпены в эфирных маслах и могут быть получены искусственно из терпенов или иным путем. Далее, терпены связаны со смолами и бальзамами, добываемыми из растений и находящими также широкое применение в медицине и технике (приготовление лаков и пр.). Применение смол и бальзамов, опирающееся на их антисептические свойства, известно было древним. Так, египтяне достигли большого искусства в бальзамировании трупов, применяя терпены, бальзамы и смолы.
К собственно терпенам примыкают вообще углеводороды, формула которых является кратной С5Н8. Таким образом, настоящие или собственно терпены будут углеводороды (C5H8)2 = C10H16. По отношению к ним углеводород С5Н8, известный в свободном виде изопрен — будет геми- ли поли-терпеном; встречающиеся в эфирных маслах углеводороды формулы С15H24 = (С5Н8)3 — полуторными или сескви-терпенами, а твердые углеводороды (С5Н8)n коллоидального характера, составляющие главную массу каучука и гуттаперчи, — поли-терпенами. Связь между изопреном, собственно терпеном и политерпенами выражается в том, что изопрен может быть получен разложением при нагревании терпена и каучука, и обратно — при действии некоторых реактивов может быть превращен в терпен и каучук.
Собственно терпены в чистом виде представляют бесцветные, подвижные, сильно преломляющие свет жидкости или твердые кристаллические тела приятного запаха, нерастворимые в воде. Терпены летучи, способны перегоняться с парами воды и прямо, причем температуры кипения разных терпенов лежат в пределах 140°-188°, а удельные веса приблизительно 0,82-0,87. Очень непостоянны; многие очень легко окисляются даже кислородом воздуха, причем воздух озонируется (благотворное влияние воздуха сосновых лесов). Оптически деятельны. Большое число изомерных терпенов, близость свойств, непостоянство чрезвычайно затрудняли изучение этих веществ. Только развитие теории строения, стереохимии, методов исследования и синтеза, открытие специальных реактивов, изучение полиметиленовых соединений, методов окисления и восстановления, общее изучение процессов изомеризации пролило свет на эту важную, интересную, но сложную область. В разработке этой области принимали деятельное участие различные ученые, особенно же: А. Байер, Валлах, Земмлер, Бредт и др. в Германии, у нас — В. Е. Вагнер, Флавицкий и др., во Франции — Бертло, Шарабо и др., в Англии — Тильден и Перкин. В настоящее время установлено, что среди терпенов имеется большое число изомеров, и некоторые из них получены синтетически.
Кроме указанных выше свойств, общих для большинства терпенов, другие химические свойства различных терпенов неодинаковы, и на основании их терпены можно разделить на группы.
Для того, чтобы уяснить возможность различных групп терпенов, следует иметь в виду следующее. Терпены удалены от предельных углеводородов CnH2n+2 на 3 пары или 6 атомов водорода, то есть имеют 3-ю степень непредельности. Каждая степень непредельности может обусловливаться или присутствием двойной связи, или цикла, причем двойная связь и цикл эквивалентны. На этих основаниях для терпенов возможны такие случаи: 1) открытая цепь углеродных атомов и три двойных связи 3 (=); 2) 1 цикл и 2 двойных связи Δ, 2 (=); 3) 2 цикла и 1 двойная связь
2Δ, 1 (=) и 4) 3 цикла и ни одной двойной связи — 3Δ. Терпены этих групп различаются по реакциям присоединения.
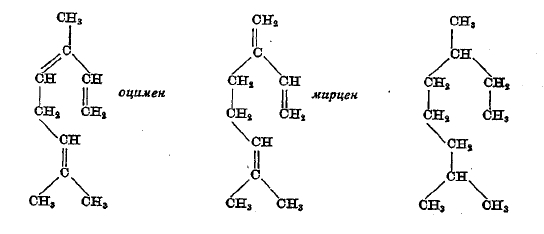
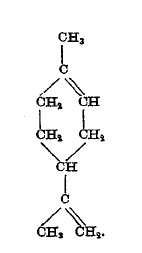
1) При присоединении к терпенам первой группы, к которой относятся мирцен и оцимен (см. внизу ст. 595/96), шести атомов или одновалентных групп получаются производные предельных углеводородов, или при присоединении водорода — предельный углеводород.
2) К терпенам второй группы присоединяются 4 атома Н, Вr, 4 группы ОН, 2 молекулы галоидоводородных кислот, 2Н2O.
3) К терпенам 3-й группы по месту двойной связи присоединяются 2 атома Н, Br, 2 группы ОН, 1 молекула галоидоводородных кислот, 1 Н2О. К некоторым терпенам присоединяются NOCl и N2O3 с образованием кристаллических соединений, для них характерных.
При присоединении водорода к терпенам 2-й группы они переходят в полиметиленовые углеводороды, именно — в пара (1,4)-метил-изопропил-гексаметилен, которому дано название ментана (см.):
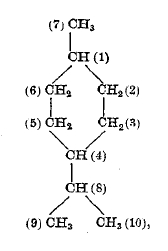
а этой группе терпенов – ментановой группы.
Только один из терпенов этой группы – сильвестрен (см. карвестрен) при восстановлении переходит в мета-изопропил-гексаметилен:
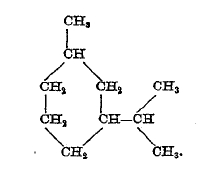
Терпены ментановой группы производятся от этих двух полиметиленовых углеводородов введением в частицу их двух двойных связей. Так как двойные связи можно расположить различно, то от каждого из приведенных полиметиленовых углеводородов можно произвести несколько терпенов. Вследствие присутствия асимметрических атомов углерода число изомеров возрастает, так как возможна оптическая изомерия. Терпены этой группы можно рассматривать также как продукты восстановления цимола (п.-метил-изопропил-бензола), в который они могут переходить при отнятии водорода.
Для краткости принято обозначать положение двойных связей символически; так, если обе двойные связи помещаются в цикле, то ставят значок Δ (цикл), а затем цифрами, отделенными запятой друг от друга, указывают атом углерода, от которого идет двойная связь; если двойная связь в боковой цепи, то положение ее отмечается двумя цифрами (из которых вторая ставится в скобках), указывающими между какими атомами углерода помещается двойная связь. Так, важнейший терпен этой группы, которого оптически недеятельная форма называется дипентеном, или карвеном, а деятельные — лимоненами (см.), будет обозначаться так: Δ1, 8(9) п.-ментадиены. Кроме лимонена, к этой группе относятся: Δ1,3 и Δ1,4 терпинен, Δ1, 4(8) терпинолен, Δ1,5 и Δ2,1(7) фелландрены; все эти углеводороды являются пара-ментадиенами, а сильвестрен Δ1, 8(9) - мета-ментадиеном:
Терпены камфановой группы могут быть произведены введением двойной связи в частицы следующих бициклических углеводородов; в которые эти терпены могут быть переведены восстановлением:
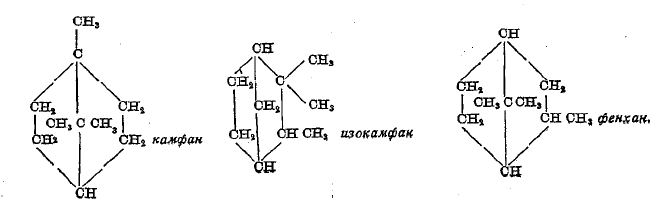
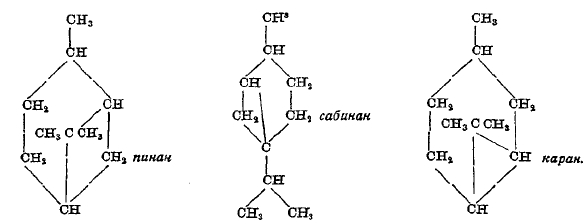
От каждого из этих углеводородов можно произвести по несколько изомеров, отличающихся положением двойной связи, но не все известны в действительности. Существуют и оптические изомеры. Наиболее важны из этой группы — пинены (см.), камфен (см.) и борнилен:
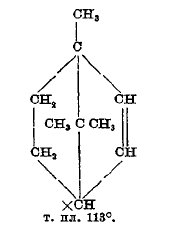
Последний интересен и важен потому, что от него (и камфана) производится борнеол и камфара. По отношению к реакциям этих углеводородов следует заметить, что те из них, которые заключают прочные пятичленные циклы, присоединяют (главным образом) по месту двойных связей, а пинен и карен иногда и по месту связи группы СН3ССН3 с 6-членным циклом с разрывом меньшего цикла. Из физических свойств этих углеводородов следует отметить сравнительно низкую температуру кипения — 140°-163° (терпены ментановой группы кипят при 173°-188°), высокую температуру плавления и большую летучесть.
Из терпенов последней группы — без двойной связи — можно указать на трициклен:
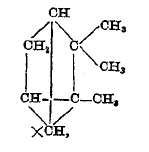
относящийся к камфену, как метил-циклопропан
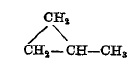
к нормальному бутилену СН3СН2СН = СН2, и некоторые другие.
Об изомерных превращениях в ряду терпенов. Терпены - соединения очень подвижные и изменчивые, легко переходящие друг в друга при разнообразных условиях: нагревании, действии реагентов, особенно кислот. Все это весьма затрудняет получение их в виде совершенно однородных соединений и определение их строения. Поэтому особенно важно по отношению к этой группе соединений установить зависимость между строением и легко и точно определяемыми физическими свойствами (особенно молекулярной рефракцией) и найти закономерности изомерных превращений простейших циклических соединений. В разработке этих вопросов русским ученым принадлежит видная роль.
Изомерные превращения терпенов могут быть подведены под следующие группы: 1) оптическая изомеризация — рацемизация; этот процесс представляет мало особенностей, поэтому будет оставлен без рассмотрения. 2) Перемещение двойной связи — также. 3) Гораздо более характерны два следующие процесса, а именно: а) переход одного цикла в другой или в двойную связь (что иногда бывает связано друг с другом) и взаимное перемещение радикалов, особенно так называемая пинаколиновая и ретропиноколиновая перегруппировка — так называется процесс, аналогичный переходу пинакона
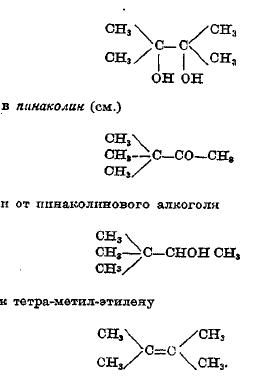
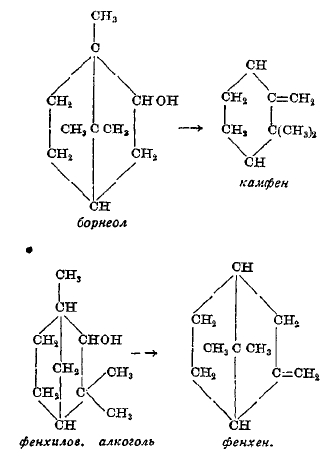
Переходы из одного цикла в другой или цикла трех- или четырехчленного в двойную связь наблюдаются среди терпенов очень часто. Переход четырехчленного цикла в пятичленный происходит при превращении пинена в камфен (через производные борнеола), а в двойную связь — при переходе пинена при нагревании в углеводороды 2-й группы (лимонен) — дипентен, терпинен, терпинолен или в производные дипентена — терпины. Переход трехчленного цикла в двойную связь происходит при превращении производных карена в сильвестрен. Наблюдаются и другие переходы циклов, особенно шестичленного в пятичленный и обратно и даже переход от бициклической системы карана в семичленный цикл. Установленная общая закономерность — изомеризация циклических углеводородов с боковой цепью СН2Х, примыкающей к циклу (Демьянов, Валлах), с образованием цикла, содержащего n + 1 атомов углерода, если взятое соединение содержало n атомов, — наблюдается и на терпенах. Изучением изомеризаций в ряду терпенов с успехом занимались также в Германии — Мервейн, у нас — С. С. Наметкин.
Кислородные соединения терпенов. Кислородные соединения - производные терпенов очень многочисленны, разнообразны и часто сопровождают терпены в эфирных маслах. Многие имеют чрезвычайно большое практическое значение. Разнообразие их вызывается различными причинами: 1) составом, то есть содержанием водорода и кислорода при 10 атомах углерода; 2) формой кислорода: гидроксил, карбонил, окисная форма и пр.; 3) положением кислорода в молекуле; 4) построением углеродного скелета, то есть структурой соответствующего углеводорода; 5) оптической и геометрической изомерией. Если вспомнить, какое большое число изомеров соответствует терпенам, встречающимся в природе, и принять во внимание, что каждому терпену или продукту его восстановления отвечает несколько (иногда много) кислородных соединений, то ясно будет, какую сложную и, благодаря изомеризации, запутанную картину представляют кислородные производные терпенов. Среди встречающихся в живой природе, часто в растениях, и получаемых синтетически кислородных соединений терпенов наиболее важны спирты, альдегиды, кетоны и окиси. Что касается связанных с терпенами кислот, то они главным образом представляют интерес для установления строения терпенов, для их синтеза, а также благодаря интересным процессам изомеризации, которые среди них часто наблюдаются.
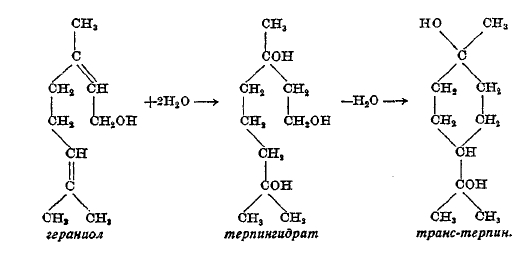
Как самим терпенам, так и углеводородам, получающимся присоединением к ним Н, отвечают спирты. Таким образом, известны спирты с открытой цепью и циклические. По числу гидрокислов они могут быть одно-, двух- и более атомными. Двухатомные — гликоли и четырехатомные — эритриты получаются в качестве первых продуктов окисления хамелеоном (по Вагнеру) углеводородов, заключающих двойные связи, в результате присоединения 2ОН по месту каждой двойной связи. Тверды, кристалличны, поэтому имеют значение для характеристики и установления формул строения терпенов; в растениях не встречаются, не имеют запаха и практического применения не находят. Но трехатомный алкоголь — терпингидрат (см.), прекрасно кристаллизующийся и получающийся при стоянии скипидара со спиртом и разведенной азотной кислотой, а также при действии на пинен кислот серной, фосфорной и др., находит медицинское применение. Он образуется присоединением 3Н2О к пинену с разрывом колец и представляет соединение с открытой цепью. Получается также присоединением 2Н2О к гераниолу:
Одноатомные спирты, альдегиды, кетоны и окиси группы терпенов. Гораздо важнее, чем многоатомные спирты, спирты одноатомные, представляющие обыкновенно жидкости приятного запаха, часто встречающиеся в эфирных маслах и вообще в растениях. Известны спирты состава C10Н20O, С10H18О и С10Н16О. Из спиртов состава С10Н20О укажем на два первичных спирта:
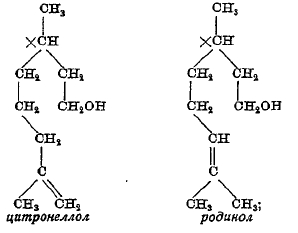
им отвечают альдегиды: цитронеллаль и родиналь (вместо группы СН2ОН в альдегидах группа ![]() ).
).
Из спиртов той же формулы замкнутого строения следует указать на ментол (см.). Ментолу отвечает кетон – ментон (см.). От ментана, замещая водород (на ОН) в других группах, можно произвести и еще спирты того же состава (всего 2 первичных, 2 вторичных, 2 третичных, не считая стереоизомеров). Переходим к спиртам состава С10Н18О. Из моноциклических соединений (ментановой группы) заслуживают внимания терпинеолы (ментенолы, см. скипидар). При отнятии от них воды получается дипентен. Рядом с терпинеолом при действии серной кислоты на терпингидрат образуется немного цинеола (см.), представляющего окись, отвечающую cis-терпину.
Кроме терпинеолов, известно большое число других спиртов, отвечающих лимонелу, терпинену, терпинолену, сильвестрену и другим моноциклическим терпенам, но они особого интереса не представляют и широкого применения не нашли.
Среди спиртов, являющихся производными бициклических углеводородов, несомненно наиболее важным является борнеол, или борнейская камфара (и стереоизомерный с ним изоборнеол), который может быть добыт из скипидара – из пинена (с изомеризацией) и при окислении переходит в кетон – японскую, настоящую камфару (см.).
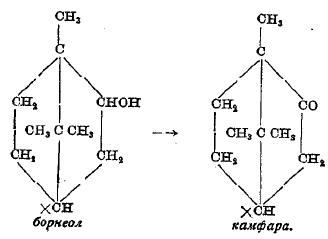
Борнеол и камфара представляют только наиболее ярких представителей обширной группы алкоголей и нейтральных продуктов их окисления, являющихся производными бициклических терпенов. Кроме спиртов, альдегидов и кетонов, в растениях встречаются нейтральные кислородные производные терпенов и другого того химического характера, а именно — представляющие кислородные гетероциклы. Сюда относятся: упомянутый выше цинеол, представляющий окись cis-терпина; пинол С10Н16О — окись собрерола С10Н18(ОН)2, двухатомного спирта, образующегося при окислении пинена с разрывом четырехчленного цикла; а также недавно открытый в эфирном американском масле (Chenopodium ambrosioides) аскаридол, С10Н16О, получивший название потому, что он является прекрасным специфическим средством против глистов (аскарид). Аскаридол — жидкость отвратительного запаха и вкуса кипит при 83° при 4-5 мм. Если его нагревать под обыкновенным давлением, то раньше, чем закипеть, он разлагается весьма бурно (взрыв) и даже самовоспламеняется. На основании химических свойств: нейтрального характера, отсутствия реакций альдегидов и кетонов (группы С = О), весьма легкого восстановления в двухатомный спирт — пара-ментандиол (1,4)
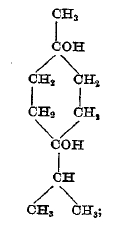
Аскаридолу придают следующее строение:
Группа сескви-терпены не менее терпенов распространена в эфирных маслах. Углеводороды имеют формулу С15Н24. С углеводородами связаны и часто сопровождают их кислородные соединения с тем же числом атомов углерода. Хотя некоторые представители этой группы известны давно, но отношения в этой группе еще более сложны и запутаны, чем в группе терпенов собственно (С10Н16). Вследствие этого строение сескви-терпенов еще далеко не выяснено, и синтез их не осуществлен. По физическим свойствам соединения этой группы отличаются от производных сескви-терпенов более высокими температурами кипения и удельным весом. По строению они, как и терпены, могут быть с открытой цепью, одно- и многоядерными. В качестве примеров можно указать на углеводороды этой группы: кариофиллен, температура кипения 132-134° (при 16 мм), d020 = 0,9035; кадинен в можжевеловом масле и др., температура кипения 274-275°, d20 = 0,918, [n]0 = 1 50647, [α]0 = -98,6°. Оба терпена принадлежат к группе бициклических соединений.
Н. Демьянов.
| Номер тома | 41 (часть 7) |
| Номер (-а) страницы | 594 |
